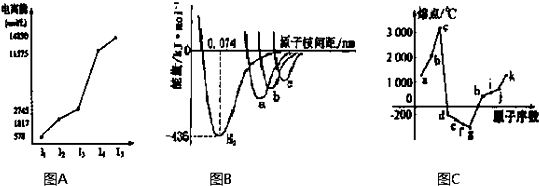
电离能是指气态原子或气态离子失去一个电子所需要的最小能量,常用符号I表示.I1表示第一电离能,I2表示第二电离能,依此类推.现有5种元素,A、B、C、D、E,其中有三种金属元素,一种稀有气体元素,其I1~I3分别如下表.根据表中的数据判断其中的金属元素有 ,稀有气体元素有 ,最活泼的金属是 ,显二价的金属是 .
| 元素 | I1/eV | I2/eV | I3/eV |
| A | 13.0 | 23.9 | 40.0 |
| B | 4.3 | 31.9 | 47.8 |
| C | 5.7 | 47.4 | 71.8 |
| D | 7.7 | 15.1 | 80.3 |
| E | 21.6 | 41.1 | 65.2 |
下列说法中不正确的是( )
| A、元素的第一电离能是元素的单质失去最外层1个电子所需要吸收的能量,同周期从左到右元素的第一电离能逐渐增大 | B、元素的电负性用来描述不同元素的原子对键合电子吸引力的大小,电负性越大的原子对键合电子的吸引力越大 | C、一般来说,周期表从左到右,元素的电负性逐渐变大;周期表从上到下,元素的电负性逐渐减小 | D、鲍林的电负性是以氟的电负性为4.0作为相对标准得出各元素的电负性(稀有气体未计) |
下列各组元素按电负性递增排列的一组是( )
| A、Na,K,Rb | B、Si,P,N | C、O,S,Cl | D、N,P,As |
下列有关电负性的说法中正确的是( )
| A、主族元素的电负性越大,元素原子的第一电离能一定越大 | B、在元素周期表中,元素电负性从左到右越来越大 | C、金属元素电负性一定小于非金属元素电负性 | D、在形成化合物时,电负性越小的元素越容易显示负价 |
下列各项叙述中,正确的是( )
| A、Ge的电负性为1.8,则其是典型的非金属 | B、L层不含s能级,M层存在3f能级 | C、焰火是焰色反应,都是电子由基态跃迁到激发态的结果 | D、在电子云示意图中,小黑点是电子在原子核外出现的概率密度的形象描述 |
电子排布有能级顺序,若以E(nl)表示某能级的能量,以下各式中正确的是( )
| A、E(4s)>E(3d)>E(3Px)>E(3Py) | B、E(3d)>E(4s)>E(3p)>E(3s) | C、E(5s)>E( 4f)>E(3Px)=E(3Py) | D、E(5s)>E(4s)>E( 4f)>E(3d) |
下面的排序不正确的是( )
| A、电负性的大小:Cl>S>Al>Mg | B、硬度由大到小:金刚石>碳化硅>晶体硅 | C、熔点由高到低:石英>食盐>干冰>钠 | D、晶格能由大到小:NaF>NaCl>NaBr>NaI |
下列对各组物质性质的比较中,正确的是( )
| A、第一电离能:Na<Mg<Al | B、熔点:金刚石>晶体硅>碳化硅 | C、硬度:Li>Na>K | D、空间利用率:六方密堆<面心立方<体心立方 |