根据键能数据估算Si(s)+O2(g)=SiO2(s)的反应热△H为( )
| 化学键 | Si-O | Si-Si | O=O | Si-C |
| 键能/(kJ/mol) | 460 | 176 | 498 | 155[ |
| A、-246kJ?mol-1 |
| B、+246kJ?mol-1 |
| C、-990kJ?mol-1 |
| D、+990kJ?mol-1 |
下列图示与对应的叙述相符的是( )
A、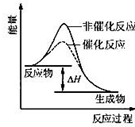 表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | B、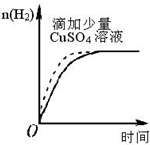 表示常温下,等量锌粉与足量的等浓度的盐酸反应(滴加CuSO4溶液的为虚线) 表示常温下,等量锌粉与足量的等浓度的盐酸反应(滴加CuSO4溶液的为虚线) | C、 表示 KNO3的溶解度曲线,a点所示的溶液是 80℃时 KNO3 的不饱和溶液 表示 KNO3的溶解度曲线,a点所示的溶液是 80℃时 KNO3 的不饱和溶液 | D、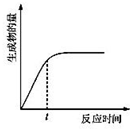 表示某可逆反应生成物的量随反应时间变化的曲线,t 时反应物转化率最大 表示某可逆反应生成物的量随反应时间变化的曲线,t 时反应物转化率最大 |
科学家发现,不管化学反应是一步完成或分几步完成,该反应的热效应是相同的,已知在25℃、1.0×105Pa时,1molC(石墨)完全燃烧生成CO2气体,放热393.5KJ,1molCO完全燃烧生成CO2气体,放热283.0KJ,下列说法正确的是( )
| A、在25℃.1.0×105Pa时,1molC(石墨)不完全燃烧,生成CO气体的热化学方程式是2 C(石墨)(s)+O2(g)═2CO(g);△H=-110.5kJ | B、1molC(石墨)不完全燃烧,生成CO与CO2混合气体时,放热283.3KJ | C、C(石墨)与CO2(g)反应生成 CO(g)的反应是吸热反应 | D、如果金刚石燃烧生成CO2的反应放热大于石墨燃烧生成 CO2放出的热,则可以断定从石墨转变为金刚石的变化需要放热 |
在298K,101kPa时,1mol物质完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热.一些烷烃的燃烧热如表:下列表达正确的是( )
| 化合物 | 燃烧热(kJ/mol) | 化合物 | 燃烧热(kJ/mol) |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 异戊烷 | 3531.3 |
| A、正戊烷的燃烧热大于3531.3kJ/mol |
| B、相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
| C、正丁烷转化为异丁烷的热化学方程式为:CH3CH2CH2CH3(g)═CH3CH(CH3)CH3(g)△H=+8.4kJ/mol |
| D、甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-891.0kJ/mol |
关于下列图示的说法中,正确的是( )
A、 如图表示可逆反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H>0 | B、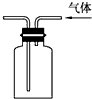 如图所示实验装置排空气法收集CO2气体 | C、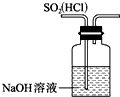 如图装置可以用来除去SO2中的HCl | D、 如图所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
下列说法正确的是( )
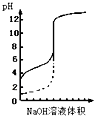

| A、△H>0的反应,常温下一定不能自发进行 | B、用0.1mol/L NaOH溶液分别滴定相同物质的量浓度和相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线 | C、等物质的量的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) | D、恒容密闭容器中进行的反应3A(g)?B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将减小 |
分析如图的能量变化示意图,下列选项正确的是( )


A、C(g)═A(g)+
| ||
| B、2C═2A+B;△H>0 | ||
| C、2A+B═2C;△H>O | ||
| D、2A(g)+B(g)=2C(g)△H<0 |
下列叙述正确的是( )
| A、吸热反应一定是反应物总能量大于生成物的总能量 | B、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | C、强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱 | D、在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
下列说法正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 | B、任何放热反应在常温下一定能发生反应 | C、放热反应不需要加热就能发生 | D、吸热反应在一定条件(如常温、加热等)下也能发生 |
下列说法正确的是( )
A、如图所示的是一个放热反应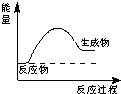 | B、加入催化剂v(正)增大、v(逆)减小 | C、燃烧热是生成1mol H2O放出的热量 | D、人们把能够发生有效碰撞的分子叫活化分子 |