已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为:
C(石墨,s)+O2(g)=CO2(g)△H=-393.51kJ/mol
C(金刚石,s)+O2(g)=CO2(g)△H=-395.41kJ/mol
据此判断,下列说法正确的是( )
C(石墨,s)+O2(g)=CO2(g)△H=-393.51kJ/mol
C(金刚石,s)+O2(g)=CO2(g)△H=-395.41kJ/mol
据此判断,下列说法正确的是( )
| A、由石墨制备金刚石是吸热反应;金刚石比石墨稳定 | B、由石墨制备金刚石是吸热反应;石墨比金刚石稳定 | C、由石墨制备金刚石是放热反应;石墨比金刚石的能量低 | D、由石墨制备金刚石是放热反应;石墨比金刚石的能量高 |
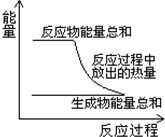 已知在101KPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-820KJ?mol-1.则下列说法中正确的是( )
已知在101KPa时:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-820KJ?mol-1.则下列说法中正确的是( )| A、反应过程中的能量变化关系可如图所示 | B、11.2LCH4完全燃烧放出热量410KJ | C、CH4的燃烧热为820KJ | D、凡是有水生成的氧化还原反应都是放热反应 |
下列反应前后物质的总能量变化不能用如图表示的是( )


| A、石灰石在高温下的分解反应 | B、生石灰和水的反应 | C、盐酸与氢氧化钠溶液的反应 | D、木炭在氧气中燃烧 |
下列说法中正确的是( )
| A、伴有能量变化的物质变化不都是化学变化 | B、物质发生化学反应不一定伴随着能量变化 | C、吸热反应在常温下不能发生 | D、放热反应的发生无需任何条件 |
 反应:2H2(g)+O2(g)═2H2O(l)过程中的能量变化如图所示,下列有关说法中正确的是( )
反应:2H2(g)+O2(g)═2H2O(l)过程中的能量变化如图所示,下列有关说法中正确的是( )| A、△H1<0 | B、△H2为该反应的反应热 | C、△H3不是H2的燃烧热 | D、△H2=△H1+△H3 |
根据热化学方程S(s)+O2(g)═SO2(g)△H=-297.23kJ/mol(反应在25℃,101kPa下发生)分析下列说法不正确的是( )
| A、形成1molSO2(g)中的化学键所释放的总能量大于断裂1molS(s)和1molO2(g)中的化学键所吸收的总能量 | B、1molS(g)充分燃烧生成SO2,放出热量大于297.23kJ | C、1molS(g)充分燃烧生成SO2(g),放出热量小于297.23kJ | D、在25℃,101kPa下,燃烧1molS放出的热量为297.23kJ |
下列说法中正确的是( )
| A、伴有能量变化的物质变化都是化学变化 | B、物质发生化学反应一定伴随着能量变化 | C、吸热反应在常温下不能发生 | D、放热反应的发生无需任何条件 |
下列说法或表示方法正确的是( )
| A、已知C(s)+O2(g)═CO2(g)△H1,C(s)+1/2O2(g)═CO(g)△H2;则△H1>△H2 | B、等量的H2在O2中完全燃烧,生成气态水比生成液态水放出的热量多 | C、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 | D、由石墨比金刚石稳定可知:C(金刚石,s)═C(石墨,s)△H>0 |
下列说法不正确的是( )
| A、反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H<0 | B、常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小 | C、在溶液中导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 | D、温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变 |
 氯原子对O3的分解有催化作用:O3+Cl═ClO+O2△H1,ClO+O═Cl+O2△H2.大气臭氧层的分解反应是:O3+O═2O2△H,该反应的能量变化如图所示,则下列叙述正确的是( )
氯原子对O3的分解有催化作用:O3+Cl═ClO+O2△H1,ClO+O═Cl+O2△H2.大气臭氧层的分解反应是:O3+O═2O2△H,该反应的能量变化如图所示,则下列叙述正确的是( )