对于反应中的能量变化,下列表述正确的是( )
| A、放热反应中,反应物的总能量大于生成物的总能量 | B、加热才能发生的反应一定是吸热反应 | C、断开化学键 的过程会放出能量 | D、氧化反应均为吸热反应 |
已知H2的燃烧热为-285.8kJ/mol,CO的燃烧热为-282.8kJ/mol.现有H2和CO组成的混合气体56.0L(标准状况),经充分燃烧后,放出的总热量为710.0kJ,并生成液态水.下列说法正确的是( )
| A、CO燃烧的热化学方程式为:2CO(g)+O2(g)═2CO2(g)△H=+282.8 kJ/mol | B、H2燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ/mol | C、燃烧前混合气体中,H2的体积分数为40% | D、燃烧后的混合气体与足量的过氧化钠反应,转移电子的物质的量为2 mol |
下列图中能正确表示X+3Y═2Z(放热反应)过程的能量变化的是( )
A、 | B、 | C、 | D、 |
已知298K时:2Al2O3(s)+3C(s)═4Al+3CO2(g)△H=2171kJ?mol-1△S=635.5J?mol-1?K-1
则此反应( )
则此反应( )
| A、常温下可自发进行 | B、温度达2000K时才可自发进行 | C、任何条件下都不可自发进行 | D、由于此反应自发进行需要的温度很高,很难达到,因此一般不用此法制铝 |
已知如下两个热化学反应方程式.
 (l)+H2(g)-→
(l)+H2(g)-→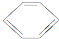 (l)△H>0 ①
(l)△H>0 ①
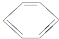 (l)+2H2(g)-→
(l)+2H2(g)-→ (l)△H<0 ②
(l)△H<0 ②
下列说法不正确的是( )
 (l)+H2(g)-→
(l)+H2(g)-→ (l)△H>0 ①
(l)△H>0 ① (l)+2H2(g)-→
(l)+2H2(g)-→ (l)△H<0 ②
(l)△H<0 ②下列说法不正确的是( )
| A、反应①、②都属于加成反应 | B、在通常条件下,反应①、②都能自发进行 | C、反应①吸热、反应②放热的事实说明苯环中含有的并不是碳碳双键 | D、反应①、②中的所有有机物均可使溴水褪色,但褪色原理不完全相同 |
 25℃、101kPa时甲醇质子交换膜燃料电池将甲醇蒸气转化为氢气的两种反应原理是:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ?mol-1
25℃、101kPa时甲醇质子交换膜燃料电池将甲醇蒸气转化为氢气的两种反应原理是:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ?mol-1②CH3OH(g)+
| 1 |
| 2 |
下列说法中正确的是( )
| A、CH3OH的燃烧热△H=-192.9kJ?mol-1 |
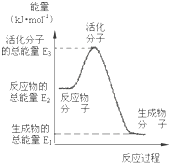
| B、反应②的能量变化如图所示,且△H2=E2-E1 |
| C、根据反应②推知:在25℃、101kPa时,1molCH3OH(l)和O2(g)反应生成CO2(g)和H2(g)放出的热量应小于192.9kJ |
| D、2H2(g)+O2(g)=2H2O(g)△H=-483.8kJ?mol-1 |
已知甲、乙、丙、丁代表4种纯净物.甲(g)+2乙(g)?丙(g)+丁(g)△H=-a kJ?mol-1(a>0),下列说法正确的是( )
| A、甲(g)的能量一定大于丙(g)的能量 | B、该反应不需要加热 | C、1 mol甲(g)与2 mol乙(g)的总能量高于1 mol丙(g)和1 mol丁(g)的总能量 | D、该反应表示:1 mol甲(g)与2 mol乙(g)在一定条件下反应放出的热量为a kJ?mol-1 |
已知:①H+(aq)+OH-(aq)═H2O(l)△H1;②2SO2(g)+O2(g)?2SO3(g)△H2.其他条件不变时,改变反应物的量,则下列判断正确的是( )
| A、△H1增大,△H2减小 | B、△H1增大,△H2增大 | C、△H1减小,△H2减小 | D、△H1不变,△H2不变 |
H2与O2发生反应的过程用模型图示如下(“-”表示化学键):下列说法不正确的是( )
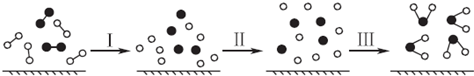

| A、过程Ⅰ是吸热过程 | B、过程Ⅲ一定是放热过程 | C、该反应过程所有旧化学键都断裂,且形成了新化学键 | D、该反应的能量转化形式只能以热能的形式进行 |
下列变化中,一定不存在化学能与热能相互转化的是( )
| A、铝热反应 | B、金属钝化 | C、干冰气化 | D、燃放爆竹 |