已知Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0;则下列关于该反应的叙述不正确的是( )
| A、反应物的总能量高于生成物的总能量 | B、上述热化学方程式中的△H的值与反应物的用量无关 | C、该反应的化学能可以转化为电能 | D、该反应中旧键断裂吸收能量,新键形成放出能量,所以物质的总能量不变 |
已知反应:2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1,下列对于反应2H2O(l)═2H2(g)+O2(g)的说法不正确的是( )
| A、吸热反应 | B、△S>0 | C、只能在电解条件下进行 | D、在一定温度下可以自发进行 |
下列说法正确的是( )
| A、加热条件下,反应NH4Cl(s)=NH3(g)+HCl(g)的△H<O、△S>O | B、水解反应Fe3++3H2O?Fe(OH)3+3H+达到平衡后,升高温度平衡正向移动 | C、氢氧碱性燃料电池放电时,正极反应为O2+4e-+4H+=2H2O | D、硫酸工业中在吸收塔里装填瓷环增大气液接触面积,以增大SO3的吸收效率 |
下列图示与对应的叙述相符合的是( )
A、图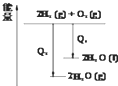 表示氢气与氧气反应中的能量变化 表示氢气与氧气反应中的能量变化 | B、图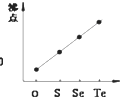 表示气态氢化物沸点 表示气态氢化物沸点 | C、图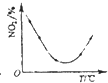 表示在容积相同的恒容密闭容器中,等量的NO2在不同温度下反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 表示在容积相同的恒容密闭容器中,等量的NO2在不同温度下反应:2NO2(g)?N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 | D、图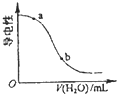 表示CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b 表示CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |
下列图示与对应的叙述相符的是( )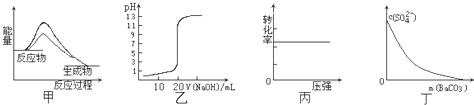

| A、图甲表示使用催化剂后,该反应的△H变小 | B、图乙表示0.10mol?L-1NaOH溶液滴定20.00mL 0.10mol?L-1CH3COOH溶液所得到的滴定曲线 | C、图丙表示反应H2(g)+I2(g)?2HI(g)中H2的转化率随压强的变化 | D、图丁表示在饱和Na2SO4溶液中逐步加BaCO3固体后,溶液中c(SO42-)的浓度变化 |
将1mol A(g)和2mol B(g)置于2L某密闭容器中,在一定温度下发生反应:A(g)+2B(g)?C(g)+D(g)△H<0,C的体积分数随时间变化如图l中曲线a所示 下列说法正确的是( )
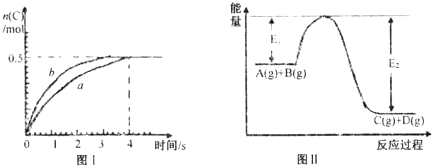

| A、此反应过程中的能量变化可用上图II表示 | B、此温度下,该反应的平衡常数的值为1 | C、该反应4s内平均速率v(A)=0.125mol?L-1?s-1 | D、若在恒温加大反应容器的容积条件下,该反应将按b曲线进行 |
关于下列过程熵变的判断不正确的是( )
| A、溶解少量食盐于水中,△S>0 | B、纯碳和氧气反应生成CO(g),△S>0 | C、H2O变成液态水,△S>0 | D、CaCO3(s)加热分解为CaO和CO2(g),△S>0 |
已知:
①101kPa下,2C(石墨,s)+O2(g)=2CO(g)△H=-221kJ?mol-1
②C(石墨,s)=C(金刚石,s)△H=-1.91kJ?mol-1
③在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1,下列有关说法正确的是( )
①101kPa下,2C(石墨,s)+O2(g)=2CO(g)△H=-221kJ?mol-1
②C(石墨,s)=C(金刚石,s)△H=-1.91kJ?mol-1
③在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1,下列有关说法正确的是( )
| A、金刚石比石墨稳定 | B、石墨的热值比9.2kJ?g-1大 | C、所有强酸与强碱反应生成1molH2O时放出的热量都为57.3kJ | D、1mol醋酸与1mol氢氧化钠在稀溶液中完全反应时,放出的热量大于57.3kJ |
下列说法中,正确的是( )
| A、放热反应不需要加热就可以发生 | B、化学反应除了生成新物质外,还伴随着能量的变化 | C、反应条件为加热的反应都是吸热反应 | D、化学反应放热还是吸热,取决于反应条件 |
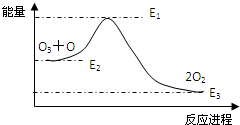 大气臭氧层的反应是:O+O3=2O2△H,该反应的能量变化如图所示,下列叙述中,正确的是( )
大气臭氧层的反应是:O+O3=2O2△H,该反应的能量变化如图所示,下列叙述中,正确的是( )| A、O+O3=2O2是吸热反应 | B、O+O3=2O2是放热反应 | C、反应O+O3=2O2的△H=E3-E2 | D、反应O+O3=2O2的△H=E3-E1 |