X、Y、Z、W 属于同周期的短周期主族元素,原子序数依次增大,它们的原子最外层电子数之和为17,且Y原子最外层电子数是X原子最外层电子数的3倍,W的内层电子数比最外层电子数多.下列说法正确的是( )
| A、原子半径大小:r(X)>r(Y);简单离子半径大小:r(W)>r(Z) | B、X、Y、Z最高价氧化物的水化物两两之间可以发生反应 | C、氢化物的稳定性:W>Z;氧化物水化物的酸性:W>Z | D、甲物质由Y和Z元素组成,溶于水后得到甲的水溶液 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )


| A、含元素Z的盐溶液一定显酸性 | B、原子半径的大小顺序为:rX>rY>rZ>rW>rQ | C、1mol CaY2与CO2反应时,转移2mol电子 | D、NaXO2溶液中加入盐酸可观察到红棕色气体 |
五种短周期元素的某些信息如表所示:
下列说法正确的是( )
| 元素 | 有关信息 |
| X | 最高价氧化物对应的水化物能与其气态氢化物反应生成盐 |
| Y | M层上有3个电子 |
| Z | 短周期元素中原子半径最大的主族元素 |
| W | 其单质是淡黄色固体 |
| Q | 最高正价与最低负价代数和为6 |
| A、简单离子的半径大小顺序为:W>Q>Z>Y |
| B、Z单质在氧气中燃烧后的产物不能使品红溶液褪色 |
| C、单质熔点高低的顺序为:Z>Y>X |
| D、Z与W元素只能形成原子个数比为2:1的化合物 |
X、Y、Z、W、M五种元素的原子序数依次增大,且X、Y、Z、W均为短周期中的非金属元素,X元素的原子形成的阴离子核外排布与氦原子相同,Z、W在周期表中处于相邻位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍,M是地壳中含量最高的金属元素.下列说法正确的是( )
| A、五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X | B、化合物X2W2、YW2、ZW2都含有极性共价键和非极性共价键 | C、工业上通常用电解熔融的MCl3来冶炼金属M | D、Z、X两元素能形成原子个数比为1:3和2:4的化合物 |
X、Y是第三周期主族元素,电负性:X>Y,下列说法错误的是( )
| A、Y的电离能一定比X的小 | B、Y的气态氢化物的稳定性一定比X的差 | C、Y的最高价含氧酸的酸性一定比X的小 | D、X与Y若形成化合物,X一定显负价 |
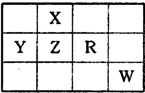 图为元索周期表前四周期的一部分,且X、Y、Z、R和W为主族元素.下列说法正确的是( )
图为元索周期表前四周期的一部分,且X、Y、Z、R和W为主族元素.下列说法正确的是( )| A、Y单质一定既能与盐酸又能与氢氧化钠溶液反应 | B、五种元素的原子最外层电子数一定都大于2 | C、单质X的熔点一定比单质Z的熔点高 | D、R的最高价氧化物对应的水化物一定是强酸 |
香花石有“国宝”之称,系1958年由中国学者在湖南香花岭锡矿发现的矿物晶体.组成香花石的元素为周期表中前20号主族元素,化学式为X3Y2(ZWR4)3T2.已知X、Y、Z为金属元素,Z原子最外层电子数与次外层电子数相等,X、Z位于同主族,Y、Z、R、T位于同周期,R原子最外层电子数为其次外层电子数的3倍,T元素无正价,X、R元素的原子序数之和是W的2倍.下列说法中不正确的是( )
| A、原子半径:X>Z>R>T | B、气态氢化物的稳定性:T>R>W | C、最高价氧化物对应水化物的碱性:Z<Y<X | D、化合物XR2和WR2中R元素的化合价相同 |
X、Y、Z、M是4种短周期主族元素,其中X与Y同主族,Y与M同周期、X与Z 同周期,X原子最外层电子数是其电子层数的3倍,Z原子的核外电子数比X原子 少1.M是同周期主族元素中原子半径最大的元素.下列说法不正确的是( )
| A、含Y元素的所有18电子微粒均可与Cl2反应 | B、Z的单质Z2的电子式为 | C、X、Y、Z元素的氢化物中,X的氢化物最稳定 | D、四种元素简单离子的半径由大到小依次为:Y>Z>X>M |
已知第三周期元素M,其原子最外层达到饱和时所需的电子数小于次外层与最内层电子数之差,且等于最内层电子数的正整数倍.下列关于元素M的说法一定错误的是( )
| A、M元素存在同素异形体 | B、M元素为非金属元素 | C、M的最高价氧化物对应的水化物都是强酸 | D、常温下,能稳定存在的M的氧化物都是酸性氧化物 |
现有短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍.下列说法正确的是( )
| A、简单阳离子的氧化性:Y>X | B、气态氢化物的稳定性:Z>M | C、简单离子半径由大到小的顺序是:Z>M>Y | D、等浓度的X2Z与Y2Z的溶液中,水的电离程度:X2Z>Y2Z |