下表是元素周期表的一部分,下列有关说法不正确的是( )
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | a | b | |||||
| 3 | c | d | e | f |
| A、元素a是制备一种高效电池的重要材料 |
| B、由b元素形成的单质不一定是原子晶体 |
| C、c、d两元素的单质构成原电池两电极时,d可能为负极 |
| D、e、f的含氧酸的酸性依次增强 |
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
| X | ||
| Y | ||
| Z | W |
| A、X对应的单质化学性质很活泼 |
| B、原子半径:W>Z>Y |
| C、Z的最高价氧化物的水化物是一种强酸 |
| D、气态氢化物的稳定性:Y<Z |
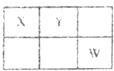 已知X、Y、W均为短周期元素,在元素周期表中的相对位置如图所示,且Y、W的质子数之和为23.下列说法正确的是( )
已知X、Y、W均为短周期元素,在元素周期表中的相对位置如图所示,且Y、W的质子数之和为23.下列说法正确的是( )| A、元素X的氧化物均为大气污染物 | B、元素Y的氧化物具有还原性 | C、元素W的氧化物对应水化物都属于强酸 | D、三种元素的原子半径:W>Y>X |
如图是元素周期表的一部分,下列说法正确的是( )
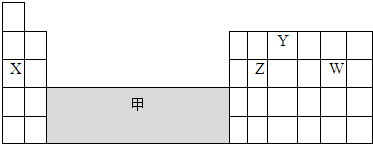

| A、可在灰色区域“甲”中寻找催化剂 | B、离子半径:W->Y3->X+ | C、气态氢化物的稳定性:Z>W | D、工业上电解X和W化合物的水溶液制备X |
几种短周期元素的原子半径及主要化合价如表:
下列说法正确的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、离子半径大小:r(M3+)<r(T2-) |
| B、其中R的金属性最强 |
| C、煤和石油中不存在X元素 |
| D、L、X形成的简单离子核外电子数相等 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断.下列说法错误的是( )
| A、若X+和Y2-的核外电子层结构相同,则原子序数:X>Y | B、硅、锗都位于金属与非金属的交界处,都可以做半导体材料 | C、由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S | D、Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH>Ba(OH)2 |
短周期元素X、Y、Z、W、Q在元素周期表的位置如表,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法正确的是( )
| X | Y | ||
| Z | W | Q |
| A、W得电子能力比Q强 |
| B、由Z与Y组成的物质在熔融时能导电 |
| C、化合物XQ4中含有σ键和π键 |
| D、WY3空间结构为平面三角形 |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,下列结论正确的是( )
| W | X | |
| Y | Z |
| A、X、Y、Z中最简单氢化物稳定性最弱的是Z |
| B、Z元素氧化物对应水化物的酸性一定强于Y |
| C、Z元素单质在化学反应中只表现氧化性 |
| D、X、Y、Z元素形成的单核阴离子还原性最强的是Y |
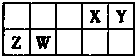 X、Y、Z、W为四种短周期元素,它们在周期表中的位置如图所示.Z元素原子核外第一层与第三层电子数相等.下列说法不正确的是( )
X、Y、Z、W为四种短周期元素,它们在周期表中的位置如图所示.Z元素原子核外第一层与第三层电子数相等.下列说法不正确的是( )| A、与相同浓度的盐酸反应,Z单质比W单质更剧烈 | B、Y元素可以形成多种具有漂白性的化合物 | C、Y与Z、Y与W形成的化合物含有的化学键类型相同 | D、四种元素的离子半径大小为Z>W>X>Y |
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中X的最高正价与最低负价绝对值之差等于2.下列判断不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中X的最高正价与最低负价绝对值之差等于2.下列判断不正确的是( )| A、最简单气态氢化物的热稳定性:Y>Z | B、最高价氧化物对应水化物的酸性:X<Z | C、X元素可与氢元素形成离子化合物 | D、已知HY沸点远高于HZ,因为H-Y键的键能高于H-Z键 |