能证明SO2具有漂白性的是( )
| A、酸性KMnO4溶液中通入SO2气体后溶液褪色 | B、滴入酚酞的NaOH溶液中通入SO2气体红色消失 | C、品红溶液中通入SO2气体红色消失 | D、溴水中通入SO2气体后溶液褪色 |
 如图所示装置,若关闭活塞,则品红溶液无变化,石蕊试液变红,澄清石灰水变浑浊.若打开活塞,则品红溶液褪色,石蕊试液变红,澄清石灰水变浑浊.据此判断该气体和广口瓶中盛放的物质分别是( )
如图所示装置,若关闭活塞,则品红溶液无变化,石蕊试液变红,澄清石灰水变浑浊.若打开活塞,则品红溶液褪色,石蕊试液变红,澄清石灰水变浑浊.据此判断该气体和广口瓶中盛放的物质分别是( )| A、CO2和浓H2SO4 | B、SO2和NaHCO3溶液 | C、Cl2和NaHCO3溶液 | D、Cl2和饱和氯化钠溶液 |
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物)其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)对PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表(H+与OH-未列出):
根据表中数据判断PM2.5的酸碱性为 ,试样的PH值= .
(2)为减少SO2的排放,常采取的措施有:
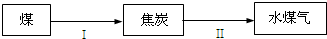
①将煤转化为清洁气体燃料.已知:H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol C(s)+
O2(g)=CO(g)△H=-110.5kJ/mol,写出焦炭与水蒸气反应的热化学方程式 ;
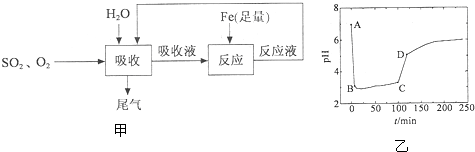
②洗涤含SO2的烟气,以下物质可作洗涤剂的是 .
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0.若气缸中进入1mol空气(1mol空气含有0.8mol N2和0.2mol O2),1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol,计算该温度下的平衡常数的数值,并写出计算过程;
②汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是 .
③汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),已知该反应的△H>0,简述该设想能否实现的依据 .
0 60038 60046 60052 60056 60062 60064 60068 60074 60076 60082 60088 60092 60094 60098 60104 60106 60112 60116 60118 60122 60124 60128 60130 60132 60133 60134 60136 60137 60138 60140 60142 60146 60148 60152 60154 60158 60164 60166 60172 60176 60178 60182 60188 60194 60196 60202 60206 60208 60214 60218 60224 60232 203614
(1)对PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表(H+与OH-未列出):
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度(mol/L) | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.已知:H2(g)+
| 1 |
| 2 |
| 1 |
| 2 |
②洗涤含SO2的烟气,以下物质可作洗涤剂的是
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化为:
①已知气缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0.若气缸中进入1mol空气(1mol空气含有0.8mol N2和0.2mol O2),1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol,计算该温度下的平衡常数的数值,并写出计算过程;
②汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是
③汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),已知该反应的△H>0,简述该设想能否实现的依据
 某化学兴趣小组用以下装置探究SO2的某些化学性质.
某化学兴趣小组用以下装置探究SO2的某些化学性质. Ca2++
Ca2++ ClO-+
ClO-+ SO2+
SO2+ H2O=
H2O=
 Cl-+
Cl-+ SO42-+
SO42-+