某学生用NaHCO3和KHCO3组成的混合物样品与某种浓度的盐酸反应进行实验,测得数据如下表:
分析表中数据,下列说法中不正确的是( )
| 实验编号 | ① | ② | ③ |
| 盐酸体积/mL | 50 | 50 | 50 |
| M(混合物)/g | 9.2 | 26.56 | 36.8 |
| V(CO2)(标准状况)/L | 2.24 | 4.48 | 4.48 |
| A、由①、②可知:①中的盐酸过量 |
| B、由②、③可知:混合物的质量增加,而气体体积没有变化,说明盐酸已经反应完全 |
| C、所用盐酸的物质的量浓度为0.4 mol?L-1 |
| D、该混合物中NaHCO3的物质的量分数为50% |
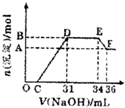 研究发现,硝酸越稀,还原产物中氮元素的化合价越低.某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出.在反应结束后的溶液中,逐滴加入4mol/LNaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.分析上述图形,下列说法不正确的是( )
研究发现,硝酸越稀,还原产物中氮元素的化合价越低.某同学取适量的铁铝合金与足量很稀的硝酸充分反应,没有气体放出.在反应结束后的溶液中,逐滴加入4mol/LNaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.分析上述图形,下列说法不正确的是( )| A、欲测定F点沉淀的质量,实验步骤是:过滤、洗涤、干燥、称量 | B、溶液中结合OH-能力最强的离子是H+,最弱的离子是Al3+ | C、溶液中n(NH4+)=0.012mol | D、OC段离子反应方程式:H++OH-=H2O |
将15.2gFe、Cu组成的合金溶于过量的稀硝酸中,生成4.48LNO(标准状况),向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为( )
| A、33.2g | B、25.4g | C、22.4g | D、19.6g |
向Cu和Cu2O的混合物27.2g中加入某浓度的硝酸0.1L,固体物质完全反应,生成NO2、N2O4、NO 和Cu(NO3)2.在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,溶液恰好呈中性,金属离子也已完全沉淀,沉淀质量为39.2g.以下所得结论不合理的是( )
| A、硝酸的物质的量浓度为12.0mol/L | B、产生的气体在标准状况下的体积为13.44L | C、Cu与Cu2O 的物质的量之比为2:1 | D、Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |
用NaHCO3和KHCO3组成的混合物分别与三份同浓度的盐酸进行反应,测得数据如下:
则下列结论中不正确的是( )
| 100mL盐酸 | 100mL盐酸 | 100mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
| A、盐酸物质的量浓度为3.0 mol/L |
| B、15.7 g混合物与盐酸反应后有剩余 |
| C、加入9.2 g混合物时消耗HCl 0.1 mol |
| D、混合物中NaHCO3和KHCO3的质量比为1:1 |
 常温下,某200mL稀硫酸和稀硝酸的混合溶液最多能溶解 19.2g铜粉(已知硝酸只被还原为NO气体),若再取等体积的该混合酸向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列有关分析错误的是( )
常温下,某200mL稀硫酸和稀硝酸的混合溶液最多能溶解 19.2g铜粉(已知硝酸只被还原为NO气体),若再取等体积的该混合酸向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列有关分析错误的是( )| A、原混合酸中NO3-的物质的量为0.2mol | B、原混合酸中H2SO4物质的量浓度为2mol/L | C、取25mL原混合酸加水稀释至1L后溶液的pH=1 | D、OA段与BC段反应中电子转移的物质的量之比为3:1 |
向xmL2.0mol/L的盐酸中投入ag镁铝合金,金属完全溶解,再加入ymL1.0mol/L的NaOH溶液沉淀达到最大值,且质量为(a+1.7)g,则下列说法不正确的是( )
| A、x=2y | B、镁铝合金与盐酸反应时转移电子的数目为0.1NA | C、镁铝合金与盐酸反应产生H2的体积在常温常压下大于1.12L | D、a的取值范围为0.9g<a<1.2g |
将一定量的NaOH和NaHCO3的混合物X放在密闭容器中加热,充分反应后生成V1 L 气体Z(V1≠0).反应后的固体残渣Y与过量的稀盐酸反应,又生成V2 L气体Z(V1、V2均为标准状况下气体的体积).下列判断错误的是
( )
( )
| A、Y的成分为Na2CO3 | ||
| B、Z的成分为CO2 | ||
| C、V1>V2 | ||
D、X中n(Na+)=
|
在14.0g银铜合金中加入500mL一定浓度的浓硝酸,合金全部溶解,收集到NO2和NO体积共2.24L(标准状况下),再向该溶液中加入bml,4mol/L的NaOH溶液,刚好使溶液中的阳离子沉淀完全;若将收集到的气体全部与标准状况下的O21.12L充分混合后,通入水中二者刚好完全反应.下列有关说法不正确的是( )
| A、银的质量为10.8g | B、NO与NO2的体积比之比(相同条件下)为2:1 | C、原硝酸的物质的量浓度(0.1mol+4b×10-3mol)/0.5L | D、沉淀中Cu(OH)2的物质的量为0.05mol |