在混合体系中,确认化学反应先后顺序有利于问题的解决,下列反应先后顺序判断正确的是( )
| A、在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+ | B、在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:Fe3+、Cu2+、H+、Fe2+ | C、在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:KOH、Ba(OH)2、BaCO3、K2CO3 | D、在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32- |
下列说法中,正确的是( )
| A、利用铁加入硫酸铜溶液中的反应可以比较Cu、Fe2+的还原性 | B、足量的铜跟一定量的浓硝酸反应只产生一种气体 | C、氮的固定只有在高温、高压、催化剂的条件下才能实现 | D、以铁为阴极、铜片为阳极、硫酸铜为电镀液可以实现铁制品镀铜 |
已知还原性 I->Fe2+>Br-,在只含有I-、Fe2+、Br-溶液中通入一定量的氯气,关于所得溶液离子成分分析正确的是(不考虑Br2、I2和水的反应)( )
| A、I-、Fe3+、Cl- | B、Fe2+、Cl-、Br? | C、Fe2+、Fe3+、Cl- | D、Fe2+、I-、Cl- |
反应Cl2+H2→2HCl可以爆炸的方式剧烈进行,该实验充分证明( )
| A、1mol Cl2的能量高于1mol HCl | B、Cl2的氧化性强于H2 | C、1mol Cl2的能量高于1mol H2 | D、Cl2的氧化性强于HCl |
下列进行性质比较的实验,不合理的是( )
| A、比较Cu、Fe的还原性:铜加入硫酸铁溶液中 | B、比较氯的非金属性强于溴:溴化钠溶液中通入氯气 | C、比较高锰酸钾的氧化性强于氯气:高锰酸钾中加入浓盐酸 | D、比较镁的金属性强于铝:取一小段去氧化膜的镁带和铝片,分别加入1.0mol?L-1的盐酸中 |
在如图所表示的微粒中,氧化性最强的是( )
A、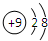 | B、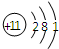 | C、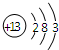 | D、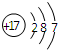 |
依据2Fe2++Cl2=2Fe3++2Cl,HClO+HCl=Cl2+H2O,2Fe3++Cu=2Fe2++Cu2+,Fe+Cu2+=Fe2++Cu判断下列氧化剂的氧化性强弱顺序正确的是( )
| A、Fe3+>HClO>Cl2>Fe2+>Cu2+ | B、HClO>Cl2>Fe3+>Cu2+>Fe2+ | C、Cl2>HClO>Fe3+>Cu2+>Fe2+ | D、Fe3+>Cu2+>Cl2>HClO>Fe2+ |
根据以下反应:
①H2S+I2=2H++2I?+S↓;
②H2SO3+2H2S=3S↓+3H2O;
③2I?+Br2=2I2+2Br?;
④H2SO3+I2+H2O=H2SO4+HI
试确定Br-、I-、H2S和H2SO3的还原性由强到弱的顺序( )
①H2S+I2=2H++2I?+S↓;
②H2SO3+2H2S=3S↓+3H2O;
③2I?+Br2=2I2+2Br?;
④H2SO3+I2+H2O=H2SO4+HI
试确定Br-、I-、H2S和H2SO3的还原性由强到弱的顺序( )
| A、H2S>H2SO3>I ?>Br? | B、Br?>I?>H2SO3>H2S | C、H2SO3>H2S>Br?>I ? | D、I ?>Br?>H2S>H2SO3 |
(CN)2、(SCN)2的化学性质与卤素单质很相似,化学上称之为拟卤素.它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-.下列有关反应的叙述中不正确的是( )
| A、Cl2通入NaCN溶液中有(CN)2生成 | B、(CN)2在碱液中能生成CN-和CNO- | C、NaBr和KSCN的混合液中加入足量的(CN)2,有Br2和(SCN)2生成 | D、在化学反应中,(CN)2、(SCN)2可作氧化剂 |
根据下列反应:I2+SO2+2H2O═H2SO4+2HI,2FeCl2+Cl2═2FeCl3,2FeCl3+2HI═2FeCl2+2HCl+I2,判断有关物质的还原性依次减弱的顺序是( )
| A、SO2、I-、Fe2+、Cl- | B、Cl-、Fe2+、SO2、I- | C、Fe2+、I-、Cl-、SO2 | D、I-、Fe2+、Cl-、SO2 |