铊盐与氰化钾被列为A级危险品,铊(Tl)与铝同主族,原子序数为81,Tl3+与Ag在酸性介质中发生反应:Tl3++2Ag=Tl++2Ag+,且已知Ag++Fe2+=Ag+Fe3+.则下列推断正确的是( )
| A、Tl+最外层有3个电子 | B、氧化性:Tl3+>Ag+>Fe3+ | C、还原性:Tl+>Ag | D、铊位于第五周期第ⅢA族 |
常温下,在下列溶液中发生如下反应:①16H++10Z-+2XO4-═2X2++5Z2+8H2O ②2A2++B2═2A3++2B-
③2B-+Z2═B2+2Z-,则下列反应中能进行的是( )
③2B-+Z2═B2+2Z-,则下列反应中能进行的是( )
| A、A3++Z-→Z2+A2+ | B、A3++X2++H2O→A2++XO4-+H+ | C、XO4-+A2++H+→X2++A3++H2O | D、B2+X2++OH-→B-+XO4-+H2O |
下列化学用语所表示的粒中,氧化性最强的是( )
A、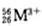 | B、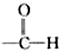 | C、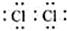 | D、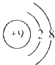 |
在盛有KMnO4溶液的试管中加入过量的MnSO4溶液,产生黑色沉淀,溶液由紫红色变为无色.过滤,在滤液中加入少量的铋酸钠粉末(NaBiO3),溶液变紫红色.另取少量酸性KMnO4溶液,加入双氧水,产生大量气泡,紫红色消失.下列推断不正确的是( )
| A、氧化性:BaBiO3>KMnO4>MnO2>H2O2 | B、用标准浓度的KMnO4溶液可以滴定溶液中Mn2+浓度 | C、在KMnO4和双氧水的反应中,KMnO4作氧化剂 | D、在铋酸钠粉末中滴加双氧水,一定会产生氧气 |
下列排列顺序正确的一组是( )
| A、半径:Fe(OH)3胶粒>I->K+>Na+ | B、熔沸点:HF<HCl<HBr<HI | C、还原性:Fe3+>Cu2+>Fe2+>Zn2+ | D、热稳定性:HF<PH3<H2S<HCl |
工业上由二氧化锰制备高锰酸钾可分为两步进行:下列说法正确的是( )
(1)二氧化锰与氢氧化钾共熔并通入氧气:
2MnO2+4KOH+O2
2K2MnO4+2H2O;
(2)电解锰酸钾溶液:2K2MnO4+2H2O
2KMnO4+H2↑+2KOH.
(1)二氧化锰与氢氧化钾共熔并通入氧气:
2MnO2+4KOH+O2
| ||
(2)电解锰酸钾溶液:2K2MnO4+2H2O
| ||
| A、根据(1)可推知,MnO2氧化性强于O2 |
| B、根据上述过程,每生成1molKMnO4共转移6mol电子 |
| C、第二步电解时,KMnO4在阳极区生成 |
| D、第二步电解时阴极周围pH减小 |
下列排列顺序正确的是( )
①沸点:H2S>H2O
②氧化性:Cu2+>Fe3+>H+>Fe2+
③原子半径:Na>Mg>O
④还原性:F->Cl->S2-
⑤结合H+的能力:OH->CH3COO->Cl-.
①沸点:H2S>H2O
②氧化性:Cu2+>Fe3+>H+>Fe2+
③原子半径:Na>Mg>O
④还原性:F->Cl->S2-
⑤结合H+的能力:OH->CH3COO->Cl-.
| A、①③④ | B、②③ | C、③⑤ | D、②④⑤ |
稀土金属元素铈(Ce)在空气中易氧化变暗,受热时燃烧,遇水很快反应.已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2.下列说法正确的是( )
| A、在一定条件下,电解熔融状态的CeO2制Ce,在阴极获得铈 | ||||||||
B、铈溶于氢碘酸的化学方程式可表示为:Ce+4HI
| ||||||||
| C、用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+═Ce3++2Fe3+ | ||||||||
D、四种稳定的核素
|
某反应中有六种微粒:Co2O3、H2O、Cl2、H+、Cl-和Co2+,已知氧化性Co2O3>Cl2.下列叙述不正确的是( )
| A、氧化产物为Cl2 | B、微粒的还原性Cl->Co2+ | C、氧化剂与还原剂的物质的量之比为1:6 | D、若有3mol H2O生成,则反应中有2mol电子转移 |
已知有以下反应:①2FeCl3+2KI=2FeCl2+2KCl+I2;②2FeCl2+Cl2=2FeCl3 ③I2+SO2+2H2O=H2SO4+2HI,下列说法正确的是( )
| A、还原性:I->Fe2+>Cl->SO2 | B、氧化性:I2>Fe3+>H2SO4>Cl2 | C、氧化性:Cl2>Fe3+>I2>H2SO4 | D、还原性:SO2>I->Fe2+>Cl- |