从矿物学资料查得,一定条件下自然界存在如下反应:
14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4
则关于该反应的说法正确的是( )
14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4
则关于该反应的说法正确的是( )
| A、Cu2S既是氧化产物又是还原产物 | ||
| B、5mol FeS2发生反应,有10mol电子转移 | ||
| C、FeS2只作还原剂 | ||
D、产物中的SO
|
在pH=1的某溶液中,可能存在NO
、I-、Fe3+中的一种或两种,向该溶液中滴入Br2,单质Br2被还原,由此推断该溶液里,上述三种离子中一定存在的离子为( )
- 3 |
A、NO
| ||
B、只有NO
| ||
| C、I-、Fe3+ | ||
| D、只有I- |
黑火药爆炸后产物为K2S、N2、CO2,下列物质中为黑火药主要成分且做还原剂的是( )
| A、氧气 | B、木炭 | C、硫磺 | D、硝酸钾 |
物质氧化性、还原性的强弱,不仅与物质的性质有关,还与物质的浓度、温度、反应物用量等有关.下列各组物质中由于浓度、温度、用量等条件不同而能发生不同氧化还原反应的是( )
①Cu与HNO3溶液;②Fe与HCl溶液;③Zn与H2SO4溶液;④铝与NaOH溶液; ⑤FeI2与Br2水; ⑥NH3与Cl2.
①Cu与HNO3溶液;②Fe与HCl溶液;③Zn与H2SO4溶液;④铝与NaOH溶液; ⑤FeI2与Br2水; ⑥NH3与Cl2.
| A、全部 | B、①③④⑥ | C、①②④⑤ | D、①③⑤⑥ |
As2S3和HNO3有如下反应:As2S3+10HNO3═2H3AsO4+3S+10NO2+2H2O,下列说法正确的是( )
| A、该反应的氧化产物仅为S | B、生成1molH3AsO4时.转移电子个数为10NA | C、将反应设计成一原电池,则NO2应该在正极附近逸出 | D、反应产生的NO2与56LO2混合在水中正好完全反应生成硝酸 |
对反应14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4的下列说法正确的是( )
| A、该反应的氧化剂只有CuSO4 | ||
| B、SO42-既不是氧化产物也不是还原产物 | ||
C、1 mol CuSO4还原了
| ||
| D、被还原的S和被氧化的S的质量比为7:3 |
已知5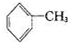 +6KMnO4+9H2SO4=3K2SO4+6MnSO4+14H2O+( )下列说法不正确的是( )
+6KMnO4+9H2SO4=3K2SO4+6MnSO4+14H2O+( )下列说法不正确的是( )
 +6KMnO4+9H2SO4=3K2SO4+6MnSO4+14H2O+( )下列说法不正确的是( )
+6KMnO4+9H2SO4=3K2SO4+6MnSO4+14H2O+( )下列说法不正确的是( )A、氧化产物为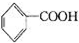 | B、 作氧化剂 作氧化剂 | C、每1mol KMnO4转移5mol e- | D、H2SO4起酸的作用 |
下列说法中正确的是( )
| A、NH3的水溶液可以导电,说明NH3是电解质 | B、标准状况下,6.72LNO2气体与水完全反应转移电子数为1.204×1023 | C、向水中通入氯气发生反应的离子方程式为:Cl2+H2O=2H++Cl-+C1O- | D、加入铝片能放出H2的溶液中可能大量共存的离子:Na+、NO3-、NH4+、SO42- |
已知:
①向盛有稀H2SO4试管中加入Fe粉,Fe粉完全溶解得浅绿色溶液;
②向实验①浅绿色溶液中滴加NaOH溶液,生成白色沉淀并立即变为红褐色;
③向实验②红褐色沉淀中滴加溶有淀粉的HI溶液,红褐色沉淀溶解得蓝色溶液.
下列判断正确的是( )
①向盛有稀H2SO4试管中加入Fe粉,Fe粉完全溶解得浅绿色溶液;
②向实验①浅绿色溶液中滴加NaOH溶液,生成白色沉淀并立即变为红褐色;
③向实验②红褐色沉淀中滴加溶有淀粉的HI溶液,红褐色沉淀溶解得蓝色溶液.
下列判断正确的是( )
| A、上述实验中,共涉及四个氧化还原反应 | B、实验可证明还原性:H+>Fe2+>OH->I- | C、实验②可证明溶解度:Fe(OH)3>Fe(OH)2 | D、实验③中,反应的离子方程式是:2Fe(OH)3+2I-+6H+=2Fe2++I2+6H2O |
多硫化钠Na2Sx(x≥2)在NaOH溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的物质的量之比为1:16.Na2Sx在结构上与Na2O2相似.则下列有关说法正确的是( )
| A、1mol Na2Sx参加反应,有32mol电子转移 | B、Na2Sx含有离子键和极性共价键 | C、该反应中Na2Sx是氧化剂,NaClO是还原剂 | D、Na2Sx中的x数值为2 |