在用容量瓶稀释浓硫酸的过程中,下列操作可引起所配溶液浓度偏低的有( )
| A、未洗涤稀释浓硫酸时用过的烧杯和玻璃棒 | B、未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中 | C、转移前,容量瓶中含有少量蒸馏水 | D、定容时,俯视视刻度线 |
配制一定物质的量浓度的溶液时,下列操作会使所配得的溶液物质的量浓度偏高的是( )
| A、省去洗涤烧杯的步骤 | B、定容时俯视刻度 | C、定容时仰视刻度 | D、定容、摇匀、静置后发现凹液面低于刻度线又加水至刻度 |
下列说法正确的是( )
| A、欲配制1.00L 1.00mol?L-1的NaCl溶液,可将58.5g NaCl涪于1.00L水中 | B、0.1mol Na2O2与足量水反应,转移电子数为0.2NA | C、同温同压下,质量相同的SO2气体和CO2气体的体积比等16:11 | D、1.0L 1.0mol?L-1的NaAlO2水溶液中含有的氧原子数大于2NA |
用98%的浓硫酸(密度1.84g?mL-1)配制100mL 1mol?L-1的稀硫酸.现给出下列配制中可能用到的仪器如下,按使用仪器的先后顺序作出的下列排列中正确的是( )
①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒.
①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒.
| A、④③⑥⑦⑤⑥ | B、②⑥③⑦⑤⑥ | C、①③⑤⑦⑤⑥ | D、②③⑥⑦⑤⑥ |
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已吸潮 | B、有少量NaOH溶液残留在烧杯内 | C、向容量瓶内加水时液面低于刻度线即摇匀 | D、向容量瓶内加水时眼睛一直仰视液面 |
实验室欲配制480mL浓度为0.1mol?L-1的Na2CO3溶液,下列操作可以实现的是( )
| A、称量5.3g Na2CO3固体溶于480mL水配制成溶液 | B、称量5.3g Na2CO3固体溶于水配制成0.5L溶液 | C、称量5.3g Na2CO3?10H2O晶体溶于水配制成0.5L溶液 | D、称量5.3g Na2CO3?10H2O晶体溶于0.5L水配制成溶液 |
配制250mL 0.1mol?L-1的盐酸溶液时,下列实验操作会使所配制溶液浓度偏高的是( )
| A、用量筒量取浓盐酸时,用水洗涤量筒,并将洗涤液倒入烧杯中 | B、配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 | C、容量瓶内有水,未经干燥处理即配制溶液 | D、定容摇匀时发现液面低于刻线,加水至刻线 |
100mL 0.5mol/L NaOH溶液加水稀释到500mL,稀释后NaOH的物质的量浓度( )
| A、0.01mol/L | B、0.1mol/L | C、0.05mol/L | D、0.04mol/L |
实验室中需要配置2mol/L的NaCl的溶液950mL,配置时应选用的容量瓶的规格和称取的质量分别是( )
| A、950mL 111.2g | B、500mL 117g | C、1000mL 117g | D、任意规格 111.2g |
下列实验操作能实现或成功的是( )
A、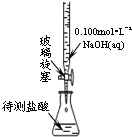 用标准液滴定待测液 | B、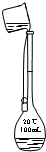 转移溶液 | C、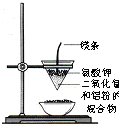 制得金属锰 | D、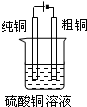 电解精炼铜 |