将质量分数为40%(密度为1.43g?cm-3)的NaOH溶液与等体积水混合,所得溶液中溶质的质量分数是( )
| A、=20% | B、<20% | C、>20% | D、≥20% |
t℃时CuSO4的溶解度为25g,将32g CuSO4白色粉末加入mg水中形成饱和CuSO4溶液并有CuSO4?5H2O晶体析出,则m的取值范围( )
| A、18 g≤m≤128 g | B、36 g<m<180 g | C、18 g<m<128 g | D、36 g≤m≤180 g |
将40℃时的饱和KCl溶液冷却至10℃,该过程中保持不变的是( )
| A、KCl的溶解度 | B、溶剂的质量 | C、溶质的质量分数 | D、溶液中K+的数目 |
影响KCl在水中的溶解度的因素是( )
| A、水的温度 | B、搅拌的速率 | C、水的体积 | D、KCl颗粒的大小 |
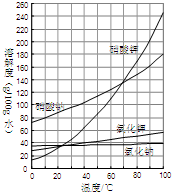 根据溶解度曲线,在80℃时含有等物质的量的硝酸钠和氯化钾混合溶液恒温蒸发,首先分析出的是( )
根据溶解度曲线,在80℃时含有等物质的量的硝酸钠和氯化钾混合溶液恒温蒸发,首先分析出的是( )| A、氯化钾 | B、硝酸钠 | C、氯化钠 | D、硝酸钾 |
下列化学实验事实及其解释都正确的是( )
| A、自然界中含钾的物质都易溶于水,是因为钾盐溶解度很大 | B、某溶液用盐酸酸化无明显现象,再滴加氯化钡溶液有白色沉淀,说明溶液中有S042- | C、铝热反应常被用于野外焊接钢轨,说明铝的氧化性很强 | D、用浓硫酸与铜在常温下可制取S02,因为浓硫酸具有强氧化性 |
一定质量某硝酸钾样品中不含可溶性杂质.在10℃时加蒸馏水使之充分溶解,残留固体的质量为250g.若该实验在40℃下进行时,残留固体质量为120g,70℃时为20g.已知KNO3在不同温度下的溶解度:
下列对该样品的推断正确的是( )
| 温度 | 10℃ | 40℃ | 55℃ | 70℃ |
| 溶解度 | 20g | 65g | 100g | 140g |
| A、样品为纯净物 |
| B、当温度在55℃时KNO3完全溶解 |
| C、70℃时的KNO3溶液为饱和溶液 |
| D、样品中可能有不溶于水的杂质 |
已知四种盐的溶解度(S)曲线如图所示,下列说法不正确的是( )
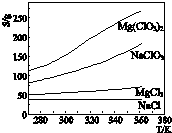

| A、将MgCl2溶液蒸干后不可能得到MgCl2固体 | B、将NaCl溶液蒸干可得NaOH固体 | C、NaClO3中混有少量NaCl杂质,可用重结晶法提纯 | D、可用MgCl2和NaClO3制备Mg(ClO3)2 |
下列有关说法中,正确的是( )
| A、某饱和溶液变成不饱和溶液,溶质的质量分数一定减小 | B、向FeSO4溶液中滴加NaOH溶液,先出现白色沉淀,最终沉淀转化成红褐色 | C、将Fe(OH)3胶体和泥水分别进行过滤,发现均有固体物质不能通过滤纸 | D、常温下,BaSO4在饱和Na2SO4溶液中的Ksp比在纯水中的Ksp小 |
将40℃的饱和澄清石灰水冷却至10℃或向其中加入少量CaO(但温度仍保持40℃),在这两种情况下均未改变的是( )
| A、溶液中溶质的物质的量浓度 | B、溶液的质量 | C、溶液中Ca2+的数目 | D、Ca(OH)2的溶解度 |