下列叙述中错误的是( )
| A、相同体积的任何气体都含有相同数目的原子 | B、标准状况下,5L H2S气体与5L NH3的原子个数比为3:4 | C、同温同压下相同体积的N2和CO气体有相同物质的量和相同的质量 | D、当粒子数相同时,气体的体积主要决定于气体粒子之间的距离 |
同温同压下,等质量的O2和SO2的.( )
| A、分子个数比为1:2 | B、密度比为1:2 | C、体积比为1:1 | D、所含原子个数比为1:1 |
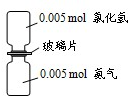 如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )
如图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )| A、气体反应物的总体积为0.224L | B、产物中所含的N-H键个数为0.015NA | C、生成物的物质的量为0.005mol | D、加水溶解后所得溶液中NH4+浓度为0.005mol?L-1 |
1811年意大利自然科学家阿伏加德罗(AmeldeoArogadro1776~1856)发现了阿伏加德罗定律,它对科学的发展,特别是相对原子质量的测定工作,起了重大的推动作用.1摩尔任何物质都含有6.02×1023个粒子,这一常数被人们命名为阿伏加德罗常数,以纪念这位杰出科学家.设 NA为阿伏加德罗常数的值,在标准状况下某O2和N2的混合气体 mg含有 b个分子,则ng该混合气体在相同状况下所占的体积应是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列物质中,所含分子数最多的是( )
| A、0.8mol CO2 | B、标准状况下22.4L氨气 | C、10.8g水 | D、3.01×1023个氯分子 |
当O2和O3的物质的量比之为3:2时,它们具有相同的.( )
| A、原子数 | B、体积 | C、摩尔质量 | D、分子数 |
只给出下列甲中和乙中对应的量,不能组成一个求物质的量的公式的是( )
| 甲 | 乙 | |
| ① | 物质微粒数 | 阿伏加德罗常数 |
| ② | 标准状况下气体摩尔体积 | 标准状况下气体体积 |
| ③ | 固体体积 | 固体密度 |
| ④ | 溶液中溶质的质量分数 | 溶液的体积 |
| ⑤ | 非标准状况下物质的质量 | 物质的摩尔质量 |
| A、③ | B、③④ | C、②③④ | D、③④⑤ |
与22g CO2所含分子数相等的水的质量为( )
| A、44g | B、22g | C、18g | D、9g |
下列叙述中,正确的是( )
| A、H2SO4的摩尔质量是98 | B、等物质的量的O2和O3中所含的氧原子数相同 | C、将98gH2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2mol?L-1 | D、等质量的CO与CO2中所含碳原子数之比为11:7 |
下列说法不正确的是( )
| A、等物质的量的-CH3和-OH所含电子数相等 | B、7.80 g Na2O2与5.85 g NaCl所含阴离子数相等 | C、等物质的量的C2H4和CH4中所含C-H键数相等 | D、等体积、等密度的12C18O和14N2所含质子数相等 |