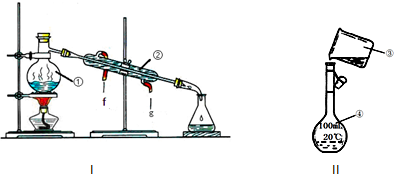
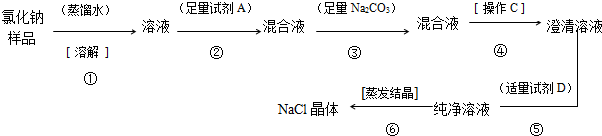
(1)下列除杂方法正确的是(括号中物质为杂质)
(2)甲同学向品红溶液中通入一种气体后,品红褪色.乙同学设计了一个简单的实验便知甲同学通入的气体是氯气还是二氧化硫.他的实验方案是: .
| 选项 | 待除杂物质 | 选用试剂 | 操作 |
| A | SiO2(CaCO3) | ∕ | 高温 |
| B | CO(O2) | Cu网 | 加热 |
| C | CO2(O2) | Cu网 | 加热 |
| D | Na2CO3(NaHCO3) | ∕ | 加热 |
| E | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
| F | Mg粉(SiO2) | NaOH溶液 | 过滤 |
已知某混合金属粉末,除铝处还含有铁、铜中的一种或两种,所含金属的量都在5%以上.请设计合理实验探究该混合物金属粉末中铁、铜元素的存在.
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液.
完成以下实验探究过程:
【提出假设】
假设1 该混合金属粉末中除铝外还含有 元素;
假设2 该混合金属粉末中除铝外还含有 元素;
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
【设计实验方案】
基于假设3,设计出实验方案(不要在答题卡上作答).
【实验过程】
根据上述实验方案,完成实验的相关操作、预期现象和结论.提示:在答题卡上按以下方式作答,注意前后内容对应.
【反思】
写出在实验①中发生反应的离子方程式: .
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液.
完成以下实验探究过程:
【提出假设】
假设1 该混合金属粉末中除铝外还含有
假设2 该混合金属粉末中除铝外还含有
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
【设计实验方案】
基于假设3,设计出实验方案(不要在答题卡上作答).
【实验过程】
根据上述实验方案,完成实验的相关操作、预期现象和结论.提示:在答题卡上按以下方式作答,注意前后内容对应.
| 编号 | 实验操作 | 实验现象 | 结论 |
| ① | 用药匙取少许样品,加入试管A中,再用滴管取过量 |
有固体剩余,并有气泡产生 | 合金中除铝外还含有Fe、Cu 元素 |
| ② | 往试管A的剩余固体中加过量 |
固体部分溶解,并有气体放出,溶液呈浅绿色 | |
| ③ | 往试管B中加入少量 |
||
| ④ | 往②剩余固体中加入稀硝酸;再滴加 |
固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色;再加某溶液后有蓝色沉淀产生 |
写出在实验①中发生反应的离子方程式:
除去下列各粉末状混合物中的杂质(括号内物质为杂质),请按下列提供的试剂和操作,将序号填在下表内.
试剂:A.盐酸;B.烧碱溶液;C.氧气;D.水;E.二氧化碳;F.不需要其他试剂.
操作:①加热;②过滤;③蒸发;④蒸馏;⑤结晶;⑥萃取
试剂:A.盐酸;B.烧碱溶液;C.氧气;D.水;E.二氧化碳;F.不需要其他试剂.
操作:①加热;②过滤;③蒸发;④蒸馏;⑤结晶;⑥萃取
| 混合物 | 试剂 | 操作 |
| Fe2O3(SiO2) | ||
| NaCl(SiO2) | ||
| SiO2(CaCO3) | ||
| SiO2(H2SiO3) |
请填写下表中除去杂质的试剂及操作方法:
| 物质 | 杂质 | 试剂 | 主要操作 |
| SiO2 | Fe2O3 | ||
| CO2 | CO | ||
| NaCl | MgCl2 | ||
| Cl2气体 | HCl |
Ⅰ.现在四种化学仪器:A.量筒 B.容量瓶 C.滴定管 D.烧杯
(1)标有“0”刻度的化学仪器为 ;(填代号,下同)
(2)实验时,要用所装液体润洗的是 ;
(3)使用前要检验是否漏水的仪器 ;
(4)量取液体体积时,平视时读数为n mL,仰视时读数为x mL,俯视时读数为y mL,若x<n<y,则所用的仪器为 .
Ⅱ.某实验小组欲从硫酸铜和硫酸亚铁的酸性混合溶液中分离出硫酸亚铁溶液,经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH值如下表:
实验室有下列试剂可供选择:H2O2、CaO、CuO、稀H2SO4、铁粉
(1)分离实验的实验操作步骤和目的为:
(2)步骤4中需要的玻璃仪器为 、 、 ;检验沉淀洗涤干净的操作方法为 .
(1)标有“0”刻度的化学仪器为
(2)实验时,要用所装液体润洗的是
(3)使用前要检验是否漏水的仪器
(4)量取液体体积时,平视时读数为n mL,仰视时读数为x mL,俯视时读数为y mL,若x<n<y,则所用的仪器为
Ⅱ.某实验小组欲从硫酸铜和硫酸亚铁的酸性混合溶液中分离出硫酸亚铁溶液,经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH值如下表:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
(1)分离实验的实验操作步骤和目的为:
| 实验步骤 | 实验操作 | 实验操作目的 |
| 步骤1 | ||
| 步骤2 | ||
| 步骤3 | ||
| 步骤4 | 洗涤沉淀 | |
| 步骤5 | 得到FeSO4溶液 |
下表所列物质(括号内为少量杂质),在(1)中选择试剂,在(2)中选择操作的方法.填表(填入序号):
(1)A.NaCl细颗粒B.NaOH溶液 C.水 D.CaO E.饱和Na2CO3 F.溴水 G.KMnO4溶液
(2)①变性 ②渗析 ③蒸馏 ④分液 ⑤结晶 ⑥洗气 ⑦过滤.
(1)A.NaCl细颗粒B.NaOH溶液 C.水 D.CaO E.饱和Na2CO3 F.溴水 G.KMnO4溶液
(2)①变性 ②渗析 ③蒸馏 ④分液 ⑤结晶 ⑥洗气 ⑦过滤.
| 物质 | 加入试剂 | 操作方法 |
| 苯(苯甲酸) | ||
| 乙酸乙酯(乙酸) | ||
| 乙烷(乙烯) |
下表所列物质(括号内为少量杂质),在B中选择试剂,在C中选择操作的方法.填表(填入序号):
B:(1)NaCl细颗粒;(2)NaOH溶液;(3)水;(4)CaO;(5)饱和Na2CO3;(6)溴水;
(7)KMnO4溶液.
C:(1)变性;(2)盐析;(3)蒸馏;(4)分液;(5)结晶;(6)洗气.
0 59480 59488 59494 59498 59504 59506 59510 59516 59518 59524 59530 59534 59536 59540 59546 59548 59554 59558 59560 59564 59566 59570 59572 59574 59575 59576 59578 59579 59580 59582 59584 59588 59590 59594 59596 59600 59606 59608 59614 59618 59620 59624 59630 59636 59638 59644 59648 59650 59656 59660 59666 59674 203614
B:(1)NaCl细颗粒;(2)NaOH溶液;(3)水;(4)CaO;(5)饱和Na2CO3;(6)溴水;
(7)KMnO4溶液.
C:(1)变性;(2)盐析;(3)蒸馏;(4)分液;(5)结晶;(6)洗气.
| 物质 | 加入试剂 | 操作方法 |
| ①苯(苯甲酸) | ||
| ②乙烷(乙烯) | ||
| ③肥皂(甘油) | ||
| ④乙醇(水) | ||
| ⑤乙酸乙酯(乙酸) |