将绿矾(FeSO4.7H2O)隔绝空气条件下强热分解,已知产物全部为氧化物,为探究绿矾分解的反应产物,某同学进行了以下实验:
实验一:为探究固体产物中Fe元素的价态,该同学将固体产物溶于足量的稀H2SO4得到相应溶液,进行以下猜想和实验
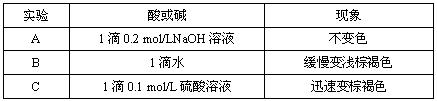
| 猜想 | 实验操作 | 预期现象 |
| 猜想一:Fe元素只显______价 | ①向所得溶液中滴入KSCN溶液 ②向稀酸性KMnO4溶液中滴入所得溶液 | KSCN溶液无明显现象 |
| 猜想二;Fe元素只显______价 | 稀酸性KMnO4溶液颜色_____ | |
| 猜想三:Fe元素既有+2价又有+3价 | KSCN溶液呈______色 稀酸性KMnO4溶液颜色______ |
实验二:为进一步探究该反应的产物,进行了如下图所示的实验
①实验开始时,点燃B处酒精喷灯之前应先打开A处活塞通CO2,其目的是
。
②装置图中C的作用是 。
③该组同学称取了55.6克绿矾按如图装置进行试验,待绿矾分解完全后,测得D瓶中沉淀的质量为23.3克,根据这些数据,可以得知,绿矾分解的化学方程式为_____________
④该组同学设计的装置存在着一个明显的缺陷是


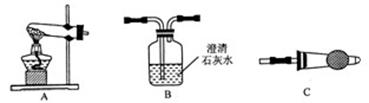

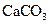 广泛存在于自然界,是一种重要的化工原料。大理石主要成分为
广泛存在于自然界,是一种重要的化工原料。大理石主要成分为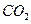 气体。下列装置可用于
气体。下列装置可用于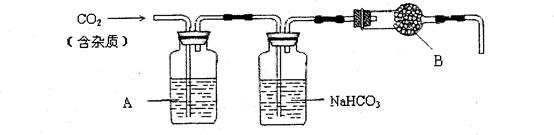
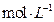 ),应选用的仪器是_____。
),应选用的仪器是_____。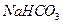 溶液可以吸收_____。
溶液可以吸收_____。 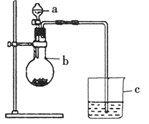
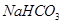 和
和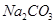 的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。
的稳定性,设计了如图甲的实验装置(铁架台、夹持仪器、加热装置等已省略),你认为在X中应放的物质_____________________(填化学式)。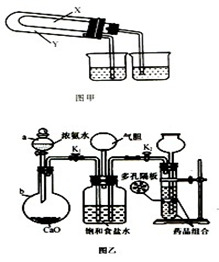
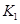 、
、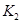 的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。
的合理顺序应为:先打开______,后打开________(填字母代号)。 简述理由____________________________。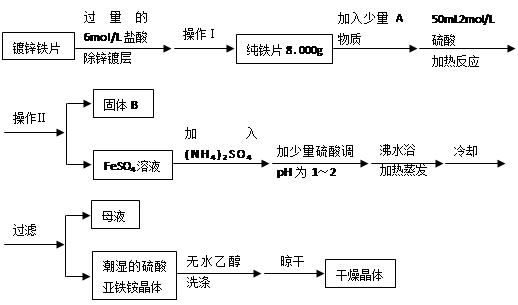
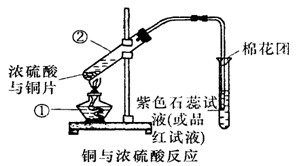
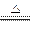 CuSO4+SO2↑+2H2O,如图是铜与浓硫酸反应的实验装置图,请回答下列问题。
CuSO4+SO2↑+2H2O,如图是铜与浓硫酸反应的实验装置图,请回答下列问题。