(8分)如何用所提供的试剂和方法除去混合物中的杂质(括号内为杂质)。将所选答案的编号填入表内相应的空格中(不需要外加试剂的,此格可标“——”,可重复选择)
I.可供选择的试剂:
| A.盐酸 | B.NaOH溶液 | C.CuO | D.饱和的NaHSO3溶液 |
| | 混合物 | 所用试剂 | 主要操作 |
| (1) | BaSO4(I2) | | |
| (2) | CaCO3(SiO2) | | |
| (3) | SO2(HCl) | | |
| (4) | CO2(CO) | | |
(8分)请选用适当的试剂和分离方法除去下列物质中所含的杂质(括号内为杂质),将所选的试剂及分离方法的编号填入表中。
试 剂:a.水 b.NaOH溶液 c.溴水 d.饱和Na2CO3溶液 e.新制CaO
分离方法:①分液 ②过滤 ③洗气 ④蒸馏
| 混合物 | 需加入的试剂 | 分离方法 |
| 溴苯(溴) | | |
| 乙烷(乙烯) | | |
| 乙醇(水) | | |
| 乙酸乙酯(乙酸) | | |
(2分)现有四种试剂:
| A.新制Cu(OH)2悬浊液; | B.浓硝酸; | C.AgNO3溶液; | D.碘水。为了鉴别下列四瓶无色溶液,(其他实验条件略)请你选择合适的试剂,将其填入相应的括号中。 |
(3) 淀粉溶液 ( ) (4) 鸡蛋清溶液 ( )
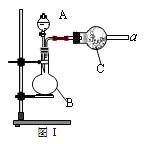
(14分)(Ⅰ)混合物的分离与提纯在化学实验中占有重要的位置。下图表示从固体混合物中分离X的方案,请回答有关问题。
(1)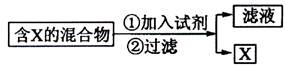
若按照以上图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是 ,有关反应的化学方程式为 ;
(2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作) 。
(Ⅱ)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。
(1)该工艺的中间过程会发生反应: ,反应的氧化剂是______________,氧化产物为__________
,反应的氧化剂是______________,氧化产物为__________
(2)在精炼铜的过程中,电解液中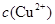 逐渐下降,
逐渐下降,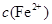 、
、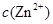 会逐渐增加,所以需定时除去其中的
会逐渐增加,所以需定时除去其中的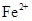 、
、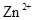 。下表为几种物质的溶度积。
。下表为几种物质的溶度积。
| 物质 |  | 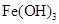 | 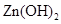 |  |
溶度积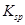 | 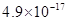 | 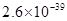 | 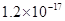 | 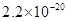 |
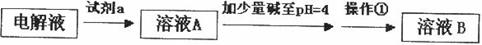
①试剂a是__________,其目的是____________________________________;根据溶度积该方案能够除去的杂质金属阳离子是____________。写出检验该杂质金属阳离子的操作方法:____________________________________________________________________________.
②乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水
调节pH至7~8,可使
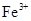 生成
生成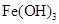 。沉淀而除去。”乙同学认为甲同学的方案中也
。沉淀而除去。”乙同学认为甲同学的方案中也应该将溶液pH调至7~8。你认为乙同学的建议是否正确?________(填“是”或“否”),
理由是________________________________________________________________________。


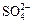 、
、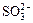 、Cl-、Br-、
、Cl-、Br-、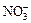 、
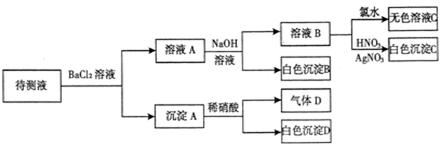
、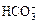 中的一种或若干种,进行下列实验(每次实验所加试剂均足量):
中的一种或若干种,进行下列实验(每次实验所加试剂均足量):