下列分离方法不合理的是 ( )
| A.从石油中得到汽油,可用蒸馏的方法 |
| B.提取溴水中的溴,可用加入乙醇萃取的方法 |
| C.只含有泥沙的粗盐,可通过溶解、过滤、结晶的方法提纯 |
| D.除FeCl2溶液中的少量FeCl3,可用加入足量铁悄过滤的方法 |
某溶液中含有HCO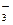 、SO
、SO 、SiO
、SiO 、Cl-等四种离子,若向其中加入某种试剂后,发现溶液中仅有HCO
、Cl-等四种离子,若向其中加入某种试剂后,发现溶液中仅有HCO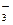
 、SO
、SO 两种离子数目大量减小。则加入的试剂可能是
两种离子数目大量减小。则加入的试剂可能是
| A.盐酸 | B.过氧化钠 | C.双氧水 | D.氯化钡溶液 |
有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述正确的是
| A.还原剂与氧化剂的物质的量之比为1︰8 |
| B.若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+ |
| C.若有lmolNO3-发生氧化反应,则转移8mole- |
| D.该过程说明Fe( NO3)2溶液不宜加酸酸化 |
某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能得到的正确结论是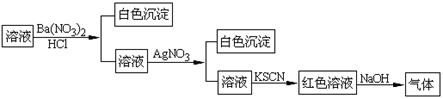
| A.原溶液中一定含有SO42-离子 | B.原溶液中一定含有NH4+离子 |
| C.原溶液中一定含有Cl-离子 | D.原溶液中一定含有Fe3+离子 |
某无色溶液中只可能含有①Na+ 、②Ba2 +、③Cl一、④Br一、⑤SO32一、⑥SO42一离子中的若干种(忽略水电离出的H+、OH-),依次进行下列实验,且每步所加试剂均过量,观察到的现象如下。
下列结论正确的是
| A.肯定含有的离子是③④⑤ | B.肯定没有的离子是②⑤ |
| C.可能含有的离子是①⑥ | D.不能确定的离子是③⑥ |
某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润红色石蕊试纸变蓝。由该实验能得到的正确结论是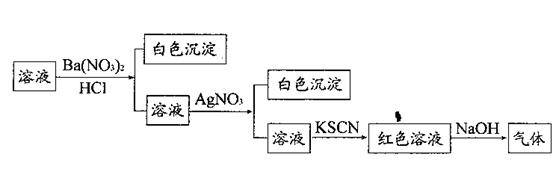
( )
| A.原溶液中一定含有SO42-离子 | B.原溶液中一定含有NH4+离子 |
| C.原溶液中一定含有Cl-离子 | D.原溶液中一定含有Fe3+离子 |
草酸晶体(2C2O4·2H2O)受热易分解:①将分解产物先通过干燥的冷的烧杯(发现产生水珠);②然后将生成的气体通入澄清石灰水中,石灰水变浑浊。甲、乙同学认为草
|
乙:H2C2O4·2H2O
| A.再验证剩余气体是否可燃及燃烧时火焰的颜色 |
| B.将剩余气体还原热的CuO粉末,观察固体颜色的变化 |
| C.将剩余气体通入溴水中,看溴水是否褪色 |
| D.将剩余气体干燥后燃烧,再用无水硫酸铜检验燃烧产物 |
检验溶液中是否含有Cl-,选用的试剂是稀硝酸和AgN O3溶液,其中稀硝酸的作用是( )
O3溶液,其中稀硝酸的作用是( )
| A.加速反应的进行 | B.排除某些杂 质离子的干扰 质离子的干扰 |
| C.生成不溶于水的物质 | D.加大沉淀的生成量 |
某有色气体可能含NO2、CH4、CO2、HCl、NH3、Br2(g)等气体中的一种或几种,为确定其组成,进行以下操作:①通少许于水中,得无色溶液;②通少许于AgNO3溶液中,有沉淀产生;③通少许于澄清石灰水中,无浑浊现象;④通过装有水的洗气瓶,导出的气体再通人澄清石灰水,产生浑浊。则可判断
| A.一定存在NO2、Br2、HCl | B.一定不存在Br2、NH3、CH4 |
| C.一定存在NO2、HCl、CO2 | D.可能存在NH3、CH4 |
下列曲线图(纵坐标为沉淀的量,横坐标为加入物的量)与对应选项不正确的是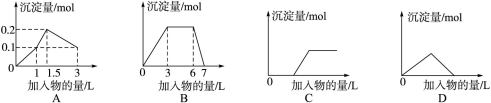
| A.向1 L浓度均为0.1 mol·L-1的Ba(OH)2、Na[Al(OH)4]混合液中加入0.1 mol·L-1稀H2SO4溶液 |
| B.向含有0.1 mol·L-1 AlCl3和0.3 mol·L-1 NH4Cl的1 L混合液中加入0.1 mol·L-1 NaOH溶液 |
| C.向烧碱溶液中滴加明矾溶液 |
| D.向Ca(OH)2溶液中逐渐通入二氧化碳 |