工业上合成氨是在一定条件下进行如下反应:
N2(g)+3H2(g)?2NH3(g),△H=-92.44kJ/mol;其部分工艺流程如下:
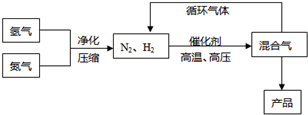
反应体系中各组分的部分性质见下表:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
(1)写出该反应的化学平衡常数表达式:K=______.随着温度的升高,K值______(填增大、减小、不变).
(2)平衡常数K值越大,表明______(填序号).
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(3)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程.即反应后通过把混合气体的温度降低到______使______分离出来;继续循环的气体是______.
 根据如图表示的一些物质或概念间的从属关系,下列各项中不正确的是:
根据如图表示的一些物质或概念间的从属关系,下列各项中不正确的是:
| X | Y | Z | |
| A | 水泥 | 硅酸盐产品 | 无机非金属材料 |
| B | 胶体 | 分散系 | 混合物 |
| C | 电解质 | 离子化合物 | 化合物 |
| D | 吸氧腐蚀 | 电化学腐蚀 | 金属腐蚀 |
- A.A
- B.B
- C.C
- D.D
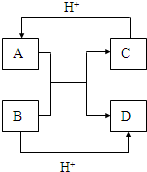 已知A、B、C、D是中学化学中常见的四种不同微粒,它们之间存在如图所示的转化关系.
已知A、B、C、D是中学化学中常见的四种不同微粒,它们之间存在如图所示的转化关系.



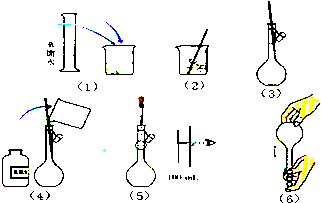
 某同学用NaCl固体配制100mL 2mol/L的NaCl溶液,请回答下列问题.
某同学用NaCl固体配制100mL 2mol/L的NaCl溶液,请回答下列问题.