下面是某同学研究维生素C过程中的一个片段,请你帮他完成相应记录.
[查阅资料]维生素C也称为抗坏血酸,是一种无色晶体,其水溶液显酸性,其化学特性是易失去电子,在水溶液中或受热时易被氧化.
[实验探究]
| 实验内容 | 实验现象 |
| 向2mL维生素C溶液中滴加2滴紫色石蕊溶液 | 溶液变为________色 |
| 将维生素C的溶液逐渐加入到2mL溶有淀粉的碘水中 | 溶液由蓝色变为无色 |
②维生素C可使食物中的Fe3+ 转化为Fe2+,这一过程体现了维生素C的________(填“氧化性”或“还原性”).③医生建议坏血病患者应多吃的食物是________(任举一种).
 直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.
直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2.
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:______.
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是______.
(3)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):______.
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
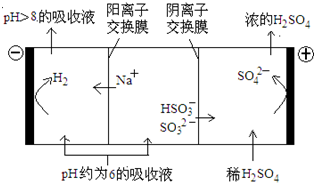
(4)当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下:
①HSO3-在阳极放电的电极反应式是______.
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用.简述再生原理:______.
在有乙离子存在的情况下,欲用试剂丙来检验溶液中是否含有甲离子,下表所加试剂丙能够对甲离子进行成功检验的是(说明:在实验过程中不允许加热、过滤、萃取等操作)
| 选项 | 试剂丙 | 甲离子 | 乙离子 |
| A | 稀硝酸、BaCl2溶液 | SO42- | SO32- |
| B | AgNO3溶液 | Cl- | I- |
| C | KSCN溶液 | Fe2+ | Fe3+ |
| D | 稀氨水 | Al3+ | Ag+ |
- A.A
- B.B
- C.C
- D.D
 4NO+6H2O
4NO+6H2O CaSiO3
CaSiO3