设NA表示阿伏加德罗常数,下列说法正确的是
- A.1molHe中有2NA个原子
- B.14g氮气中含NA个氮原子
- C.2L0.3mol/LNa2SO4溶液中含0.6NA个Na+
- D.18g水中所含的电子数为8NA
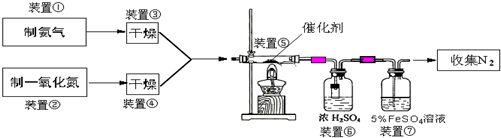
用如图装置进行实验,请回答下列问题:
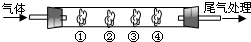
I.(1)若通入SO2气体,请填写表中空格:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 棉花浸取试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | ______ | ______ | 褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | ______ | 氧化性 |
II.若通入HCl气体,装置中的四处棉花依次做了如下处理:①包有用水润湿某固体物质、②浸有KI溶液、③浸有石蕊溶液、④浸有浓NaOH溶液.请回答:
(1)观察到②处棕黄色物质产生,则:①处包有的某固体物质可能是下列的______(填下面物质的序号),其反应的离子方程式为______.
a.MnO2 b.KMnO4 c.KCl d.Cu
(2)在实验过程中,在③处能观察到______.
(3)反应较长时间后,②处棕黄色褪去,生成无色的IO3-,该反应的离子方程式为______.