(12分)如图甲为氢氧燃料电池装置示意图(已标明电池工作时OH-的移动方向),A、B、C、D为电极。
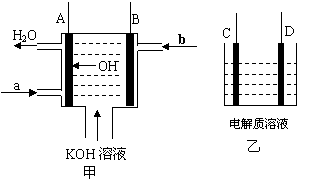 |
(1)若A、B连接外电阻并形成回路,则A电极的电极反应式 ▲ ,b处通入的气体
为 ▲ 。若乙中C为Fe、D石墨,电解质为NaCl,则导线连接C、D后,D电极
的电极反应式 ▲ 。
(2)若乙中C、D均为石墨,电解质溶液为滴有酚酞的NaCl溶液,用导线将A与D相连、
B与C相连,则一段时间后 ▲ 极附近的溶液呈红色,乙中总反应的化学方程式为 ▲_。
(3) 若乙中C为粗铜、D为纯铜片,电解质溶液为硫酸酸化的硫酸铜溶液,用导线将A与
D相连、B与C相连,则乙中D电极的电极反应式 ▲ 。当甲中b气体消耗0.1 mol
时,理论上乙中某电极增重 ▲ g
|
(1)实验原理:Fe+2H+=Fe2++H2↑。
(2)实验用品:电极(铁钉、铜钉)、
(填写电解质溶液)、 (填写所缺的实验用品)、
耳机(或者电流计)
(3)实验装置
(4)原电池设计及注意的问题
①按如图所示连接好实验仪器,注意观察(耳朵听)耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触耳机插头上的一极(注意:接触的同时耳机的另一个极是连接在原电池的另一个电极上的),这时可以听见耳机发出“嚓嚓嚓”声音。其原因是:在原电池中,由化学能转化为 ,在耳机中又由 转化为声音这种能量。
②如果将装置中的耳机改为电流计,则铁钉应该为原电池 极,电极反应式是: ;若一段时间内有3.01×1023个电子发生转移,则理论上生成标准状况下气体 L。
 C、电流的方向是从铁经导线流向铜
C、电流的方向是从铁经导线流向铜

 取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下列说法错误的是
取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下列说法错误的是