(8分)已知KMnO4和H2C2O4(草酸)在酸性溶液中会发生如下反应:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
 甲、乙两个实验小组欲探究影响化学反应速率的因素,设计
甲、乙两个实验小组欲探究影响化学反应速率的因素,设计
实验方案如下(实验中所用KMnO4溶液均已酸化):
(1)甲组:通过测定单位时间内生成CO2气体体积的量来比
较化学反应速率,实验装置如图,实验时分液漏斗中A溶
液一次性加入,A、B的成分见下表:
| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.1 mol·L-1H2C2O4溶液 | 4mL 0.01 mol·L-1KMnO4溶液 |
| ② | 2mL 0.2 mol·L-1 H2C2O4溶液 | 4mL 0.01 mol·L-1 KMnO4溶液 |
| ③ | 2mL 0.2 mol·L-1 H2C2O4溶液 | 4mL 0.01 mol·L-1 KMnO4溶液 少量MnSO4(催化剂) |
该实验探究的是 因素对化学反应速率的影响。在反应停止之前,相同时间内针筒中所得CO2的体积由大到小的顺序是 (填实验序号)。
(2)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率。
取两支试管各加入2 mL 0.1 mol·L-1H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol·L-1 KMnO4溶液。将四支试管分成两组(每组各有一支盛有H2C2O4溶液和KMnO4溶液),一组放入冷水中,另一组放入热水中,一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验试图探究
因素对化学反应速率的影响,但该组同学始终没有看到溶液完全褪色,其原因是 。
|
从化学的视角看,下列有关说法中错误的是 A.镀锡的铁制品,镀层部分受损后露出的铁表面更易腐蚀 B.减少二氧化碳的排放有利于抑制酸雨的形成 C.用尿素、硝酸钙、硝酸镁制成的新型融雪剂还能起到施肥养护树木的作用 D.利用太阳能等清洁能源代替化石燃料有利于节约资源保护环境 (14分)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。 (1)将水蒸气通过红热的碳即可产生水煤气。反应为:
①该反应能否自发进行与 有关; ②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是 (填字母,下同)。 a.容器中的压强不变 b.1 mol H—H键断裂的同时断裂2 molH—O键 c.v正(CO) = v逆(H2O) d.c(CO)=c(H2) 在该温度下,该反应的平衡常数表达式为K= . (2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
①实验1中以v(CO2) 表示的反应速率为 。 ②该反应为 (填“吸”或“放”)热反应 ③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3min,则a、b应满足的关系是 (用含a、b的数学式表示)。
a.升高温度 b.充入He(g),使体系压强增大 c.将H2O(g)从体系中分离出来 d.再充入1mol CO2和3mol H2 (12分)在一定条件下,可逆反应A + B ⑴温度T1 T2(填大于、等于或小于) ⑵正反应是 反应(填“吸热”或“放热”) ⑶如果A、B、C均为气体,则m 2(填大于、等于或小于) ⑷当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体, 则体系的压强 (填增大、减小或不变),平衡 移动(填“向正反应方向”、“向逆反应方向”或“不”) 22.
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) 回答下列问题: (1)该反应的化学平衡常数表达式为K= 。 (2)该反应为 反应(选填“吸热”、“放热”)。 (3)能判断该反应已经达到化学平衡状态的依据是 (多选扣分)。 A、容器中压强不变;B、混合气体中c(CO)不变;C、v正(H2)=v逆(H2O);D、c(CO2)=c(CO)。 (4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃ 23. (12分)在密闭容器中将NO2加热到某温度时,进行如下的反应:2NO2 ⑴NO2的转化率为? ⑵反应前后的压强比为多少? ⑶在这5分钟内,用O2来表示的平均反应速率是多少? | |||||||||||||||||||||||||||||||||||||||||||||
 A.反应I2(aq)+I-(aq)=I3-(aq)的△H>0
A.反应I2(aq)+I-(aq)=I3-(aq)的△H>0
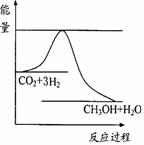 (3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g)
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g) 右图是温度和压强对
右图是温度和压强对