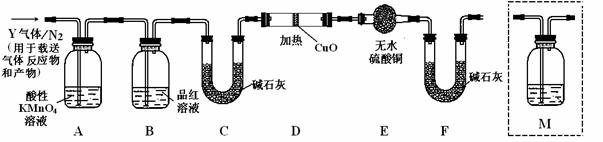
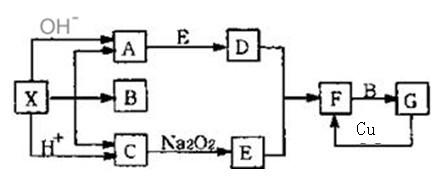
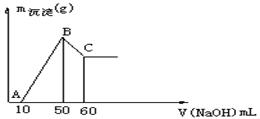
0 40410 40418 40424 40428 40434 40436 40440 40446 40448 40454 40460 40464 40466 40470 40476 40478 40484 40488 40490 40494 40496 40500 40502 40504 40505 40506 40508 40509 40510 40512 40514 40518 40520 40524 40526 40530 40536 40538 40544 40548 40550 40554 40560 40566 40568 40574 40578 40580 40586 40590 40596 40604 203614