Ⅰ.溴水和氯化铁溶液是中学化学实验中的常用试剂,浓度较小时,溶液均呈黄色。某同学将稀溴水和稀FeCl2溶液混合,所得溶液显黄色。为探究溴水和FeCl2溶液混合能否发生反应,该同学设计了以下实验方案:
| 操作 | 实验现象 | 实验结论 | |
| 方案1 | 取少量混合溶液,加入NaOH溶液,振荡 | 得到红褐色沉淀 | 发生了化学反应 |
| 方案2 | 取少量混合溶液,加入四氯化碳溶液,振荡 | 有机层呈橙黄色 | 未发生化学反应 |
| 方案3 | 取少量混合溶液,加入淀粉碘化钾溶液,振荡 | 溶液变蓝色 | 未发生化学反应 |
请回答下列问题:
(1)方案2的结论不合理,其理由是
(2)方案3的结论明显不合理,可能发生反应的离子方程式
(3)请另外设计一个简单的实验方案(包括“操作”“现象”“结论”),判断溴水和FeCl2溶液是否反应。
。
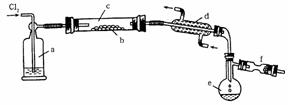 Ⅱ.S2Cl2是一种易挥发的液体(熔点:-76℃,沸点:138℃),且易与水发生水解反应,可能生成H2S、SO2、H2SO3、H2SO4等物质。它是橡胶硫化剂。在熔融的硫中通以氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。
Ⅱ.S2Cl2是一种易挥发的液体(熔点:-76℃,沸点:138℃),且易与水发生水解反应,可能生成H2S、SO2、H2SO3、H2SO4等物质。它是橡胶硫化剂。在熔融的硫中通以氯气即可生成S2Cl2。下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去)。
(1)装置a中应放试剂为__________;装置d的名称是_________,它的作用是_________。
(2)该实验的操作顺序应为__________(用序号表示)。
①加热装置c ②通入Cl2 ③通冷凝水 ④停止通Cl2 ⑤停止加热装置c
(3)将S2Cl2的水解气体产物通入氯水中,若观察到_________的现象,则可证明水解产物中有硫化氢生成。
A、B、C、D、E、F六种短周期元素的原子序数依次增大。A、D同族,B、C同周期;B原子最外层电子数是次外层的两倍;在周期表中A的原子半径最小;C是地壳中含量最多的元素,C是F不同周期的邻族元素;E和F的原子序数之和为32。由上述六种元素中的两种元素组成的甲、乙、丙、丁、戊、己六种化合物如下表所示:
元素形成的化合物
| 化合物 | 甲 | 乙 | 丙 |
| 各元素原子个数比 | n(A)∶n(C) = 2∶1 | n(A)∶n(C) = 1∶1 | n(B)∶n(A) = 1∶4 |
| 化合物 | 丁 | 戊 | 己 |
| 各元素原子个数比 | n(D)∶n(B) ∶n(C) = 2∶1∶3 | n(E)∶n(F) = 1∶3 | n(B)∶n(F) = 1∶4 |
请完成下列问题:
(1)D的离子结构示意图___________________,己的空间构型______________________。
(2)向含有1 mol 乙的水溶液中加入MnO2,该反应中电子转移的物质的量为_______mol。
(3)用离子方程式说明丁溶液的酸碱性为___________________________________________。
(4)写出由丙、C的单质、KOH溶液构成的燃料电池的负极电极反应式:_________________。


