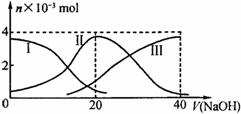
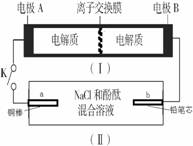
相同温度下,体积均为0. 25 L的两个恒容密闭容器中发生可逆反应:
X2(g) + 3Y2(g) ![]() 2XY3(g) △H=-92.6 kJ·mol-1
2XY3(g) △H=-92.6 kJ·mol-1
实验测得反应在起始、达到平衡时的有关数据如下表所示:
容器 编号 | 起始时各物质物质的量/mol | 达到平衡的时间 | 达平衡时体系能量的变化 | ||
X2 | Y2 | XY3 | |||
① | 1 | 3 | 0 | 2分钟 | 放热 46.3 kJ |
② | 0.4 | 1.2 | 1.2 | / | Q(Q>0) |
下列叙述不正确的是
A.容器①中反应从开始到刚达平衡时用XY3表示的反应速率为v(XY3)=1/30 mol·L-1·s-1
B.达平衡时,两个容器中XY3的物质的量浓度相等
C.容器②中反应达到平衡时吸收的热量为Q
D.若容器①体积为0.3 L,则达平衡时放出的热量大于46.3kJ
已知4NH3(g)+5O2(g) = 4NO(g) +6H2O(l) △H=-xkJ/mol。蒸发1mol H2O(l)需要吸收的能量为44kJ,其它相关数据如下表:
| NH3(g) | O2(g) | NO(g) | H2O(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | a | b | z | d |
则表中z(用x、a、b、d表示)的大小为
A.(x+4a+5b-6d-44)/4 B.(x+12a+5b-12d-264)/4
C.(x+4a+5b-6d-264)/4 D.(x+12a+5b-12d-44)/4
不论以何种比例混合,将甲和乙两种混合气体同时通入丙溶液中,一定能产生沉淀的组合是
| 序号 | 甲 | 乙 | 丙 |
| ① | HCl | CO2 | 少量偏铝酸钠 |
| ② | HCl | CO2 | 过量石灰水 |
| ③ | N2 | NH3 | 少量AgNO3 |
| ④ | CO2 | SO2 | 过量Ba(NO3)2 |
| ⑤ | CO2 | NH3 | 少量CaCl2 |
A.②③④ B. ②④ C.①③ D.②④⑤
下列实验操作与实验目的或结论都正确的是
选项 | 实验操作 | 实验目的或结论 |
A | 用干燥洁净的玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较 | 测氯水的pH |
B | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
C | 下层液体从分液漏斗下端管口放出后,关闭活塞,换一个接收容器,再将上层液体从下端管口放出 | 取出分液漏斗中的上层液体 |
D | 向某溶液中加入稀硝酸,无现象,再滴加Ba(NO3)2溶液,产生白色沉淀 | 说明该溶液中一定含有SO42- |