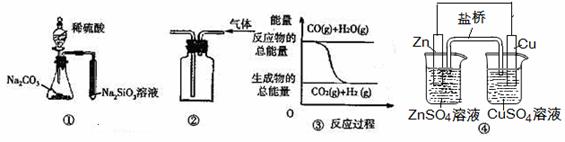
I. 实验室里用二氧化锰和浓盐酸加热制取氯气,该反应的离子方程式为: MnO2+4H++2Cl—![]() Mn2++Cl2↑+2H2O,也可以利用反应:
Mn2++Cl2↑+2H2O,也可以利用反应:
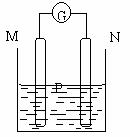
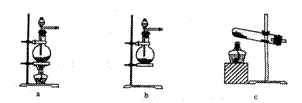
2KMnO4+16HCl(浓) 2KCl+2MnCl2+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图所示:
|
(1)若以KMnO4和浓盐酸为原料制取氯气,请根据反应原理从下图中选择合适的制气装置 (填代号)。
|
(2)装置B的作用是 。
(3)E中的试剂可选用 (填代号)。
A.NaOH溶液 B.Na2CO3溶液 C.NaCl溶液 D.水
(4)某学生通过下列两种方式制取氯气:
①用8.7gMnO2与足量浓盐酸反应制取Cl2
②用含14.6gHCl的浓盐酸与足量MnO2反应制取Cl2
这两种方式产生Cl2的量的关系是 。
A.①多 B.②多 C.①②一样多
II.现欲用碳酸钙固体和稀盐酸反应制取CO2气体,请回答下列问题:
(1)写出发生反应的离子方程式 ;
|
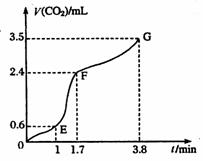
[V(CO2)]与时间(t)的关系如图
所示,试分析判断OE段、EF段、
FG段反应速率[分别用![]() (OE)、
(OE)、![]()
(EF)、![]() (FG)表示]的大小关系
(FG)表示]的大小关系
;比较OE段和EF
段,说明EF段速率变化的主要原因
应该是 。
硫代硫酸钠溶液与稀硫酸的反应方程式为:
Na2S2O3+H2SO4 = Na2SO4+S↓+SO2+H2O,
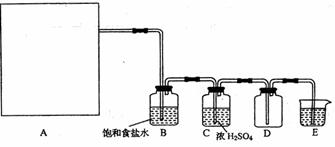
某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)。

甲 乙
(1)实验目的:装置甲,探究浓度对化学反应速率的影响;装置乙,探究 对化学反应速率的影响。
(2)通过甲、乙装置,分别进行了三组实验,数据记录如下,并经分析得出相关结论:
实验 组号 | 温度 | Na2S2O3溶液 | H2SO4 | 加入H2O的体积 | 出现沉淀所需时间 | ||
体积 | 浓度 | 体积 | 浓度 | ||||
Ⅰ | 0℃ | 5mL | 0.1mol·L-1 | 10mL | 0.1mol·L-1 | 5mL | 8s |
Ⅱ | 0℃ | 5mL | 0.1mol·L-1 | 5mL | 0.1mol·L-1 | 10mL | 12s |
Ⅲ | 30℃ | 5mL | 0.1mol·L-1 | 5mL | 0.1mol·L-1 | 10mL | 4s |
结论1:由Ⅰ和Ⅱ两组数据可知 ;
结论2:由Ⅱ和Ⅲ两组数据可知 。
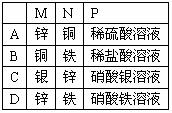
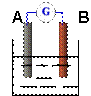 名称为 _________,写出正极的电极反应式_
名称为 _________,写出正极的电极反应式_ 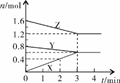 (1)该反应的化学方程式: ;
(1)该反应的化学方程式: ;