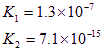25°C时,几种弱酸的电离常数如下
| 弱酸化学式 | CH3COOH | HCN | H2S |
| 电离常数(25°C) | 1.8 |
|
|
25°时,下列说法正确的是 ( )
A.等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2S)>pH(NaCN)
B.a mol/L HCN溶液与b mol/L NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定大于b
C.某浓度HCN的水溶液pH=d,则其中c(OH-)=10-dmol/L
D.NaHS和Na2S混合溶液中,一定存在c(Na+)+c(H+)===c(OH-)+c(HS-)+2c
(S2-)
有关元素X、Y、Z、W的信息如下:
| 元素 | 信息 |
| X | 所在主族序数与所在周期序数之差为4 |
| Y | 最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
| Z | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
| W | 基态原子核外5个能级上有电子,且最后的能级上只有1个电子 |
请回答下列问题:
(1)W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为
(2)铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式
(3)向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为 ,Z3+离子的电子排布式为 ,它有 个未成对电子。
(4)以上述所得WX3溶液为原料制取无水WX3,先制得WX3·6H2O晶体,主要操作包括 ,在 条件下加热WX3·6H2O晶体,能进一步制取无水WX3,其原因是(结合离子方程式简要说明) 。

 。
。 将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )
将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )