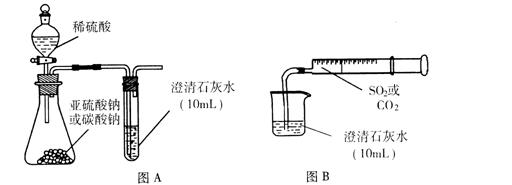
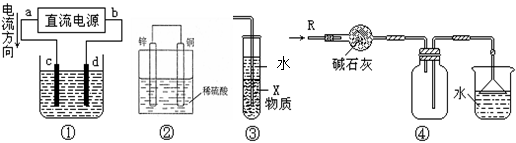
(1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:
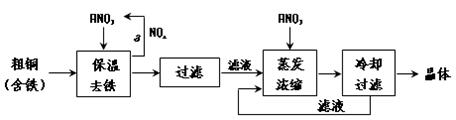
①在步骤a中,还需要通入氧气和水,其目的是 。
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在 范围。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
不用加水的方法调节溶液pH的原因是 。
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明) 。
(2)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是 。
(3)图-2是某小组同学查阅资料所绘出的硝酸铜晶体[ Cu(NO3)2·nH2O ]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是 (填字母)。

a. A点时的溶液为不饱和溶液
b. B点时两种晶体可以共存
c. 按上述流程最终得到的晶体是Cu(NO3)2·3H2O
d. 若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2·6H2O晶体
下表中的实线表示元素周期表的部分边界。①-⑥分别表示元素周期表中对应位置的元素。
| ① | ] | ||||||||||||||||
| ] | ③ | ④ | ⑤ | ||||||||||||||
| ② | ⑥ | ||||||||||||||||
| |||||||||||||||||
(1)请在表中用粗实线补全元素周期表边界。
(2)②号元素位于第 周期 族。
(3)写出由①、③两种元素组成的摩尔质量最小的化合物的电子式 ,上述元素中能和⑤号元素形成的原子晶体的化学式是
(4)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的化学反应方程式为_____________,该生成物质含有的化学键类型是 。