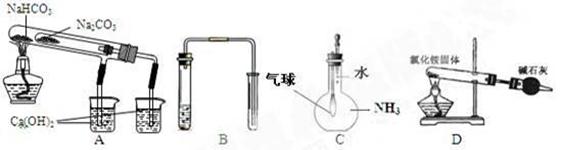
尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应如下:
2NH3(l)+CO2(g)![]() H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
试回答下列问题:
⑴下列措施中有利于提高尿素的产率的是___________。
A.采用高温 B.采用高压 C.寻找更高效的催化剂
⑵合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g)![]() H2NCOONH4(氨基甲酸铵) (l) △H1
H2NCOONH4(氨基甲酸铵) (l) △H1
第二步:H2NCOONH4(l)![]() H2O(l)+H2NCONH2(l) △H2
H2O(l)+H2NCONH2(l) △H2
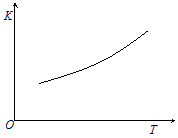
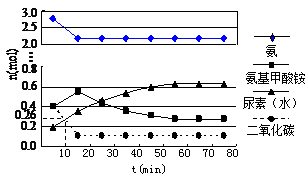 |
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:
图Ⅰ 图Ⅱ
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 ▲ 步反应决定,总反应进行到 ▲ min时到达平衡。
②反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)= ▲ 。
③第二步反应的平衡常数K随温度的变化如上右图Ⅱ所示,则△H2 ▲ 0(填“>”“<”或“=”)
现有X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素。有关信息如下表:
| 原子或分子相关信息 | 单质及其化合物相关信息 | |
| X | ZX4分子空间结构为正四面体 | X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y | Y原子的最外层电子数等于电 | Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料(人造刚玉) |
| Z | Z原子的最外层电子数是次外层电子数的 | Z是无机非金属材料的主角,其单质为原子晶体,是一种优良的半导体材料 |
| W | W原子的最外层电予数小于4 | W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(1)W位于周期表第四周期第 族,W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为 。
(2)Z最简单的氧化物分子是 分了(填“极性”或“非极性”):工业上用Z的氧化物制备其单质的化学反应方程式为 。
锗与Z是同一主族元素,门捷列夫曾预言了这一元素的存在,它最常用来制造晶体篱,最新研究表明:有机锗具有明显的抗肿瘤活性,锗元素的最高价氧化物的化学式为 。
(3)实验室制取X单质的离子方程式为 ;X的气态氧化物的水溶液与Y的氧化物反应的离子方程式为 。
(4)在50mL lmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积可能为 mL或 mL。