0 35226 35234 35240 35244 35250 35252 35256 35262 35264 35270 35276 35280 35282 35286 35292 35294 35300 35304 35306 35310 35312 35316 35318 35320 35321 35322 35324 35325 35326 35328 35330 35334 35336 35340 35342 35346 35352 35354 35360 35364 35366 35370 35376 35382 35384 35390 35394 35396 35402 35406 35412 35420 203614
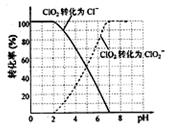 饮用水中ClO2、ClO2-的含量可用连续碘量法进行测定。
饮用水中ClO2、ClO2-的含量可用连续碘量法进行测定。