产品标准 产品等级 配料 碘含量(以Ⅰ计算) 分装日期 分装企业 | GB5461 一级 食盐、碘酸钾、抗结剂 20—50mg/kg 2007.1.25
|
1.上述精制盐属于_________(填“纯净物”或“混合物”)。
2.如果含碘量达到50mg/kg,则精制食盐中碘酸钾的质量分数为___________。
3.配平下列化学方程式。
______KIO3+______KI+______H2SO4![]() ______K2SO4+______I2+______H2O
______K2SO4+______I2+______H2O
(1)反应中作氧化剂的是________;
(2)当溶液中生成0.5 mol I2时,电子转移总数为________________个。
4.已知:I2+2![]()
![]() 2I-+
2I-+![]() 某学生测定食用精盐的碘含量,步骤为:
某学生测定食用精盐的碘含量,步骤为:
a.准确称取W g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3和KI完全反应;
c.以淀粉为指示剂,逐滴加入物质的量浓度为
2.0×10-3mol/L的Na2S2O3溶液10.0mL,恰好完全反应。
(1)判断c中反应恰好完全的依据现象是________________;
(2)b中反应所产生的I2的物质的量是________________mol;
(3)计算:根据以上实验和包装袋上的说明所测精制盐的碘含量(以含W的代数式表示)。
①将干燥的氯气在
②有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
S | 112.8 | 444.6 | 略 |
S2Cl2 | -77
| 137
| 遇水生成HCl、SO2、S; |
设计实验装置图如下:
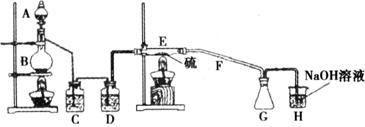
1.写出标号仪器名称:A____________、B____________;
2.B容器中反应的离子方程式____________;
3.由于S2Cl2遇水生成HCl、SO2和S,因此在G与H两装置之间增加_________装置;
4.写出所盛试剂的名称:C中__________、D中__________;
5.F仪器的名称__________,它的作用是__________;
6.如果在加热E时温度过高,对实验结果的影响是_________,在F中可能出现的现象是__________________;
7.检查整套装置气密性的方法是___________________________;
8.制得的S2Cl2粗品中可能混有的杂质是(任写一种)_________,为了提高S2Cl2的纯度,关键的操作是控制好温度和____________________________________。