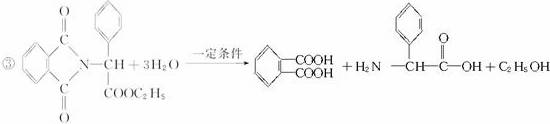
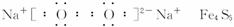二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:

某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH,见下表,回答下列问题:
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | |
pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为_________________________________。
(2)滤渣A的主要成分为_________________。
(3)加入MnS的目的是除去____________________________杂质。
(4)碱性锌锰干电池中,MnO2参与的电极反应方程式为_____________________________。
(5)从废旧碱性锌锰干电池中可以回收利用的物质有_________________(写出两种)。
在一定条件下化学反应:2SO2(g)+O2(g)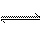 2SO3(g);ΔH=-197 kJ·mol-1。现有容积相同的甲、乙、丙三个容器,其体积保持不变,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
2SO3(g);ΔH=-197 kJ·mol-1。现有容积相同的甲、乙、丙三个容器,其体积保持不变,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
0 32037 32045 32051 32055 32061 32063 32067 32073 32075 32081 32087 32091 32093 32097 32103 32105 32111 32115 32117 32121 32123 32127 32129 32131 32132 32133 32135 32136 32137 32139 32141 32145 32147 32151 32153 32157 32163 32165 32171 32175 32177 32181 32187 32193 32195 32201 32205 32207 32213 32217 32223 32231 203614
容器 | SO2(mol) | O2(mol) | N2(mol) | Q(kJ) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | Q2 |
丙 | 1 | 0.5 | 1 | Q3 |
根据以上数据,下列叙述不正确的是
A.在上述条件下反应生成1 mol SO3气体放出热量98.5 kJ
B.Q1=2Q2=2Q3=197 kJ
C.若在上述条件下反应生成2 molSO3固体的反应热为ΔH1,则ΔH1<ΔH
D.若在甲容器中使用促进SO3生成的催化剂,则Q=Q1