名称 | 化学式 | 颜色、状态 | 溶解度(g) | 熔点(℃) | 密度(g/cm3) |
乙二酸 | H | — | 8.6(20℃) | 189.5 | 1.900 |
二水合乙二酸 | H | 无色晶体 | — | 101.5 | 1.650 |
注:乙二酸(HOOC—COOH)俗称草酸,带2个结晶水的乙二酸俗称草酸晶体,草酸晶体失去结晶水得无水草酸,在约157℃时升华,其盐草酸钙和草酸氢钙均为白色不溶物。根据上述信息,回答下列问题。
(1)向盛有Na2CO3粉末的试管里加入约3 mL乙二酸溶液,观察到的现象是________________。
(2)向盛有5 mL乙二酸饱和溶液的试管里滴入3滴用硫酸酸化的0.5%(质量分数)的高锰酸钾溶液,振荡,观察到的现象为____________,说明乙二酸有_____________性。
(3)已知草酸分解的化学方程式为:H![]() H2O+CO2↑+CO↑,用如图装置加热草酸晶体,验证草酸受热分解及其产物,但有人认为该装置不合理。请你根据草酸晶体的某些物理常数和实验目的,分析不合理原因_____________(从下列序号中选择)。
H2O+CO2↑+CO↑,用如图装置加热草酸晶体,验证草酸受热分解及其产物,但有人认为该装置不合理。请你根据草酸晶体的某些物理常数和实验目的,分析不合理原因_____________(从下列序号中选择)。
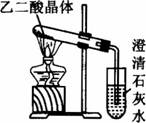
a.草酸晶体的熔点低,未分解之前就已融化并流到试管口,不利于化学反应的进行及实验现象的观察
b.因为加热的是草酸晶体,所以该装置最多只能检验一种分解产物,不能检验是否还有其他分解产物
C.在未洗气的情况下通入石灰水,还可能因草酸蒸气与石灰水反应生成草酸钙沉淀,对实验有干扰
(4)设装置也不符合绿色化学的要求,试说明原因____________________________。
(5)实验室用酸碱滴定法测定草酸晶体分子中结晶水个数的方法如下:称取a g草酸晶体溶于水配成200 mL溶液,取20 mL该溶液用0.1 mol·L-1NaOH溶液滴定,当达到终点时,用去NaOH溶液b mL,则每个草酸晶体分子中结晶水个数x=__________(用字母表示算式)。



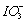 +6H+?
+6H+?