题目内容
近年来,加“碘”食盐较多地使用了强酸盐碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:KI+3H2OA.电解时,阳极反应是:I--6e-+3H2O=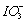 +6H+?
+6H+?
B.电解一段时间后,电解质溶液的pH几乎不变?
C.电解时,石墨作阴极,不锈钢作阳极?
D.电解过程中,当生成3 mo1 H2时,转移6 mole-?
C?
解析:KI为强酸强碱盐,水溶液呈中性、电解后pH不变,若用不锈钢作阳极,则Fe在阳极上反应失去电子。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 KIO3 + 3H2↑。下列有关说法正确的是
KIO3 + 3H2↑。下列有关说法正确的是