下表是元素周期表中的一部分。表中所列的字母分别代表某一化学元素。
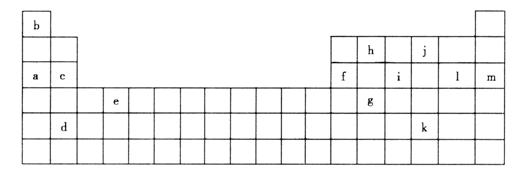
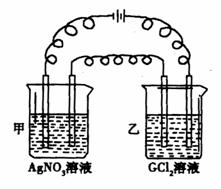
(1)下列__________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外`
电子离开该原子或离子所需要的能量主要受两大因素的影响:
a.原子核对核外电子的吸引力 b.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1)
| 锂 | X | Y |
失去第一个电子 | 519 | 502 | 580 |
失去第二个电子 | 7296 | 4570 | 1820 |
失去第三个电子 | 11799 | 6920 | 2750 |
失去第四个电子 |
| 9550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量远远大于失去第一个电子所需的量____________________。
②表中X可能为以上13种元素中的__________(填写字母)元素。用元素符号表示X和j形成化合物的化学式____________________。
③Y是周期表中__________族元素。
④以上13种元素中__________(填字母)元素原子失去核外第一个电子需要的量最多。
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理不正确的是( )
0 31808 31816 31822 31826 31832 31834 31838 31844 31846 31852 31858 31862 31864 31868 31874 31876 31882 31886 31888 31892 31894 31898 31900 31902 31903 31904 31906 31907 31908 31910 31912 31916 31918 31922 31924 31928 31934 31936 31942 31946 31948 31952 31958 31964 31966 31972 31976 31978 31984 31988 31994 32002 203614
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 |
M(混合物) | 9.2g | 15.7g | 27.6g |
VCO2(标况) | 2.24L | 3.36L | 3.36L |
A.盐酸的物质的量浓度为3.0 mol/L
B.能计算出混合物中NaHCO3的百分含量
C.加入混合物9.2 g时盐酸未反应完
D.15.7 g混合物恰好与盐酸完全反应