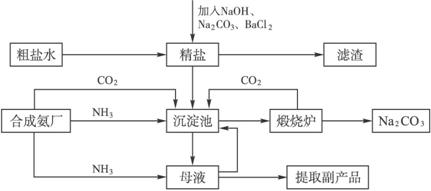
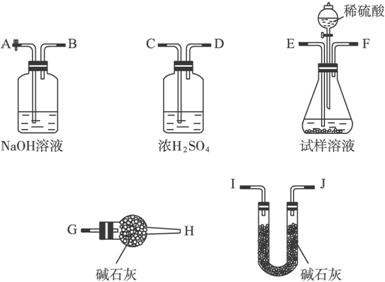
(1)请填写下表中空白,完成检验明矾中阴离子和阳离子的实验设计。
0 31485 31493 31499 31503 31509 31511 31515 31521 31523 31529 31535 31539 31541 31545 31551 31553 31559 31563 31565 31569 31571 31575 31577 31579 31580 31581 31583 31584 31585 31587 31589 31593 31595 31599 31601 31605 31611 31613 31619 31623 31625 31629 31635 31641 31643 31649 31653 31655 31661 31665 31671 31679 203614
操作 | 现象 | 结论或离子方程式 |
①取少量明矾放入烧杯中,加适量蒸馏水,并搅拌,配成稀溶液;在三支试管中分别加入约0.5 mL稀明矾溶液 | — | — |
②在第一支试管中滴加NaOH溶液至过量 | 溶液中的现象是____________ | 反应的离子方程式:______________________ |
③在第二支试管中滴加______________________________ | 溶液中有白色沉淀产生 | Ba2++ |
④对第三支试管溶液用______________________________ | _______________ | 证明有K+ |
⑤另取少量明矾晶体,放入一支干燥试管中,用酒精灯加热 | 在试管内壁和管口有水珠产生 | 证明有结晶水 |
(2)在常温下,取两片质量相等、外形相同、表面经过砂纸打磨(完全除掉了氧化膜)的铝片,分别加入到盛有相同体积、c(H+)均为3 mol·L-1的稀硫酸和稀盐酸溶液的两支试管中,发现铝片在稀盐酸中产生氢气的速率明显比在稀硫酸中快。请你对上述现象产生的原因提出假设并设计实验方案来验证你的假设。
你的假设是:假设一:__________________________;假设二:________________________。
你设计的实验方案是:______________________________。