29.化学活动课上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查)。
0 31135 31143 31149 31153 31159 31161 31165 31171 31173 31179 31185 31189 31191 31195 31201 31203 31209 31213 31215 31219 31221 31225 31227 31229 31230 31231 31233 31234 31235 31237 31239 31243 31245 31249 31251 31255 31261 31263 31269 31273 31275 31279 31285 31291 31293 31299 31303 31305 31311 31315 31321 31329 203614
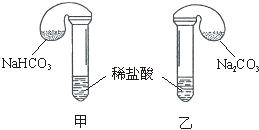
请回答:
(1)各组反应开始时,________装置中的气球体积先变大,该装置中反应的离子方程式是___________________________。
(2)当试管中不再有气体生成时,三组实验出现不同现象,填写下表的空格。
| 试剂用量 | 实验现象 (气球体积变化) | 分析原因 |
第 ① 组 | 0.42 g NaHCO3 0.53 g Na2CO3 3 mL 4 mol/L盐酸 | 甲中气球与乙中气球的体积相等 | 甲、乙盐酸均过量 n(NaHCO3)=n(Na2CO3) V甲(CO2)=V乙(CO2) |
第 ② 组 | 0.3 g NaHCO3 0.3 g Na2CO3 3 mL 4 mol/L盐酸 | 甲中气球比乙中气球的体积大 |
|
第 ③ 组 | 0.6 g NaHCO3 0.6 g Na2CO3 3 mL 2 mol/L盐酸 | 甲中气球比乙中气球的体积大 |
|
片刻后,乙中气球又缩小,甲中气球的体积基本不变 | (用离子方程式表示) |
