在100 ℃ 时,将0.100 mol 的四氧化二氮气体充入1 L 抽空的密闭容器中,发生N2O4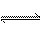 2NO2反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
2NO2反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
0 27633 27641 27647 27651 27657 27659 27663 27669 27671 27677 27683 27687 27689 27693 27699 27701 27707 27711 27713 27717 27719 27723 27725 27727 27728 27729 27731 27732 27733 27735 27737 27741 27743 27747 27749 27753 27759 27761 27767 27771 27773 27777 27783 27789 27791 27797 27801 27803 27809 27813 27819 27827 203614
时间/s 浓度 mol·L-1 | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4)/mol·L-1 | 0.100 | c1 | 0.050 | c3 | a | b |
c(NO2)/mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
(1)该反应的化学方程式为______________________________;达到平衡时四氧化二氮的转化率为__________%;表中c2__________c3__________ab__________(选填“>”“<”或“=”)。
(2)20 s时四氧化二氮的浓度c1=_________mol·L-1,在0~20 s内四氧化二氮的平均反应速率为________________mol·(L·s)-1。
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是______________mol·L-1。
 ,它属于
,它属于