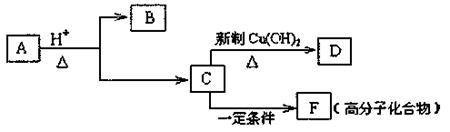
有机物A是有机合成的中间体,分子中含2个氧原子,其燃烧产物n(CO2):n(H2O)=2:1;质谱图表明A的相对分子质量为188;在一定条件下A可以转变为B和C(分子式:C4H6O),相关转化关系如下图所示
|
已知:①R—CH=CH—OH会自动转化为R—CH2—CHO;
②同一个碳原子上连有两个双键的结构不稳定;
③B苯环上的一氯取代物有两种同分异构体;C分子中无支链。
请根据以上信息,回答下列问题:
(1)A的分子式是 ,B中含氧官能团的名称是 ,F的结构简式是 。
(2)写出由C生成D的化学方程式: ;
(3)C有多种同分异构体,其中与C具有相同官能团的同分异构体(不含C)共有 种。
(4)上述转化过程中不涉及的有机反应类型有 (填序号)。
①取代反应 ②聚合反应 ③消去反应 ④氧化反应 ⑤还原反应
⑥水解反应
新华社2009年10月15日报道:全国农村应当在“绿色生态—美丽多彩—低碳节能—循环发展”的理念引导下,更好更快地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设。可见“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃,101kPa时:C(s)+![]()

则在25℃,101kPa时:C(s)+H2O(g)=CO(g)+H2(g)△H= 。
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:
FeO(s)+CO(g) ![]() Fe(s)+CO2(g)△H>0,已知在1100℃时,该反应的化学平衡常数K=0.263。
Fe(s)+CO2(g)△H>0,已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K的值 (填“增大”、“减小”或“不变”)
②1100℃时测得高炉中,c(CO2)=0.025mol·L-1,c(CO)=0.1mol·L-1,则在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是
。
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)△H=—49.0kJ·mol-1。现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g)△H=—49.0kJ·mol-1。现向体积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
|
①从反应开始到平衡,氢气的平均反应速率v(H2)= ;
②下列措施能使![]() 增大的是 (填符号)。
增大的是 (填符号)。
A.升高温度 B.再充入H2
C.再充入CO2 D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
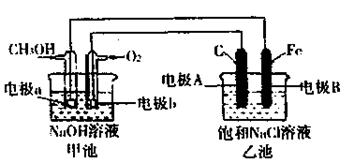
某化学过程的示意图如图所示。在装置工作过程中,甲池的总反应式为:
|
(1)甲池溶液中的Na+移向 (填“a”或“b”)电极,乙池溶液中的Na+移向
(填“A”或“B”)电极;
(2)电极A的名称: ;
(3)电极b上发生的电极反应式为 ;
(4)乙池中发生反应的离子方程式为 ;
(5)当电极A处得到0.71g产物时,甲池中理论上消耗O2 mL(标准状况下)。
化学是一门以实验为基础的自然科学,掌握实验方法以及完成化学实验所必须的技能是学好化学的关键。试回答下列实验问题:
(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图所示装置进行验证。最终该同学判定含有HCl气体的依据是:装置C中的试纸颜色无变化,装置D中产生白色沉淀(部分夹持装置和加热装置省略)
①装置B中的试剂是 ;
②装置C的作用是 。
(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废弃催化剂(主要成分为Ag/α—Al2O3)来回收金属银和α—Al2O3,部分操作过程省略。α—Al2O3作为催化剂的载体,且不溶于硝酸。
 |
①Ag/α—Al2O3加HNO溶解可选用右图
所示装置中的 (选填a、b、c);
②实验操作II中,所需的主要玻璃仪器有 ;
③实验操作II中能否用自来水代替蒸馏水? (填“能”或“否”);原因是
(结合关离子方程式回答)。
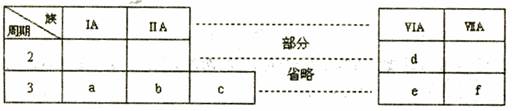
下列是元素周期表的一部分,有关说法不正确的是 ( )
|
A.a、b、d、f四种元素的离子半径:f>d>a>b
B.元素b的单质不能与酸性氧化物发生化学反应
C.元素c的氧化物既能与酸反应,又能与碱反应
D.a、c、e的最高价氧化物对应的水化物之间能够相互反应