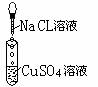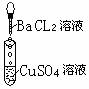饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10AL+6NaNO3+4NaOH==10NaALO2+3N2 +2H2O。请回答下列问题:
⑴上述反应中, 元素的化合价升高,则该元素的原子 (填“得到”或“失去”)电子;而 元素的化合价降低,则该元素的原子被 (填“氧化”或“还原”)。
⑵上述反应中,若有10个铝原子参与反应,则转移的电子总数为 ,用“双线桥法”表示反应中电子转移的方向和数目:
10 AL + 6 NaNO3 + 4 NaOH == 10 NaALO2 + 3 N2 ![]() + 2 H2O
+ 2 H2O
为探究离子反应的实质,某同学设计了如下实验,有关的实验现象及反应方程式
列表如下,请补充完整:
编号 | I | II | III |
实验 |
|
|
|
现象 | 有白色沉淀生成,滤液为蓝色 | 有白色沉淀生成,滴加稀硝酸,沉淀不溶解 | |
化学 方程式 |
| 2AgNO3+CuCl2==2AgCl | |
离子 方程式 |
| Ba2+ + SO42- == BaSO4 |
![]()
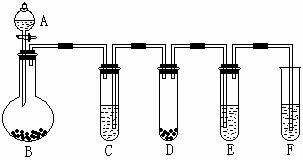
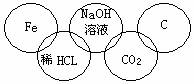
现有下列两组物质:①H2、CaCO3、HCL、NH3 ②氯化钠溶液、硫酸铜溶液、氢氧化铁胶体、硫酸铁溶液。请你从组成的元素、物质的性质等多个角度用两种不同的分类标准从每组中选出一种不同类的物质,并指出其分类依据,写在下面相应的表格内。
| 组别 | 被选出的物质 | 分类依据 |
| 第① 组 | ||
| 第②组 | ||