将甲和乙气体同时通入过量丙溶液中,可能产生沉淀的组合是( )
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | Ca(OH)2 |
| ② | HCl | CO2 | Ca(OH)2 |
| ③ | CO2 | SO2 | Ba(NO3)2 |
| ④ | NO2 | SO2 | CaCl2 |
| ⑤ | CO2 | NH3 | CaCl2 |
| ⑥ | O2 | NH3 | AlCl3 |
A.全部 B.①③④⑤⑥ C.①②③④⑤ D.①③⑤⑥
下表列有几种物质的沸点:
(1)
| 物质 | AlF3 | AlCl3 | AlBr3 | Al2O3 | MgCl2 | MgO |
| 沸点/℃ | 1260 | 181(升华) | 263 | 2045 | 707 | 2850 |
①下列各组物质中,气化或者熔化时所克服的粒子间作用力类型分别与氟化铝和溴化铝相同的是 。
A.NaCl和CCl4 B.Na2O和SiO2
C.金刚石和金属铝 D.碘和干冰
②工业上制备金属镁,应采用电解熔融的 。
A.MgCl2 B.MgO
③工业上制备金属铝,是采用电解熔融Al2O3(加冰晶石),而不是电解熔融AlCl3,原因是 。
(2)过渡元素钴(27Co)的原子核外电子排布式为 。钴有两种化学式均为Co(NH3)2BrSO4的配合物,且配位数均为6。它们分别溶解于水时电离出的阳离子的化学式可能为 和 。鉴别两者的实验方法是:分别取样并滴加 (填化学式)溶液。
(1)下表是在1.013×105Pa下测得的几种物质的沸点:
| 结构简式 | 沸点/℃ | 结构简式 | 沸点/℃ |
| CH3CH3 | -88.6 | CH2=CH2 | -103.7 |
| CH3CH2CH3 | -42.2 | CH2=CHCH3 | -47.4 |
| CH3CH2CH2CH3 | -0.5 | CH3CH2CH=CH2 | -6.3 |
|
| -11.7 |
| -6.9 |
| CH3CH2CH2CH2CH3 | 36.1 | CH3CH2CH2CH=CH2 | 30 |
|
|
| 20.1 |
从表中数据分析,![]() 在1.013×105PA.25℃时的状态是 (填气态、液态或固态)。
在1.013×105PA.25℃时的状态是 (填气态、液态或固态)。
(2)石油裂解是一个复杂的过程,其产物为混合物。例如:


①上述烷烃和环烷烃裂解反应中,产物M的化学式为 ,N的化学式为 。
②下列关于![]() 的说法正确的是 。
的说法正确的是 。
A.可用溴水区别![]() 和
和![]()
B.等质量的![]() 和
和![]() 完全燃烧时的耗氧量相同
完全燃烧时的耗氧量相同
C.![]() 可与水以任意比互溶
可与水以任意比互溶
(3)工业上裂解反应的产物都是气态小分子烷烃和烯烃的混合物,将它们逐一分离的方法是 。
从含镍废催化剂中可回收镍,其流程如下:
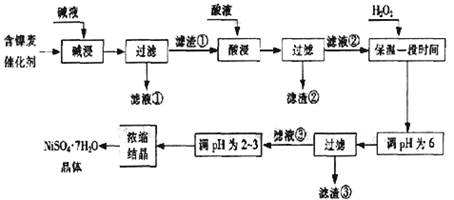
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
回答下列问题:
(1)“碱浸”的目的是除去 。
(2)“酸浸”时所加入的酸是 (填化学式)。酸浸后,滤液②中可能含有的金属离子是 。
(3)“调节pH为2~3”的目的是 。
(4)产品晶体中有时会混有少量绿矾(FeSO4?7H2O),可能是由于生产过程中
导致Fe2+未被完全氧化造成的。
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料――NiOOH。该反应的离子方程式是 。
下表是元素周期表主族元素的一部分。
| W | X | Y |
| Z |
短周期元素X的最高正价是+5价,Y单质可在空气中燃烧。
(1)Z的元素符号是 ,原子结构示意图中 。
(2)W的最高价氧化物不溶于水,但能溶于烧碱溶液,反应的化学方程式为 。
(3)探寻同一主族元素性质的一些共同规律,是学习化学的重要方法之一。在下表中列出对H2ZO3各种不同化学性质的推测,举例并写出相应的化学方程式。
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2ZO3+4HI=Z↓+2I2+3H2O |
| 1 | ||
| 2 |