题目内容
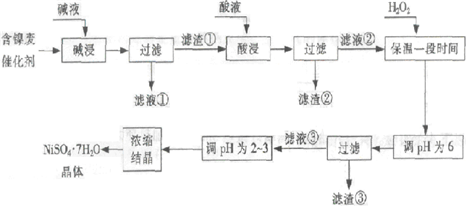
从含镍废催化剂中可回收镍,其流程如下:
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%)。部分阳离子以氢氧化物形式完全沉淀时的pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
回答下列问题:
(1)“碱浸”的目的是除去 。
(2)“酸浸”时所加入的酸是 (填化学式)。酸浸后,滤液②中可能含有的金属离子是 。
(3)“调节pH为2~3”的目的是 。
(4)产品晶体中有时会混有少量绿矾(FeSO4?7H2O),可能是由于生产过程中
导致Fe2+未被完全氧化造成的。
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料――NiOOH。该反应的离子方程式是 。
(1)Al、Al2O3、油脂
(2)H2SO4
Ni2+ 、Fe2+
(3)防止在浓缩结晶过程中Ni2+水解(或“防止在浓缩结晶过程生成Ni(OH)2沉淀)
(4)H2O2的用量不足(或H2O2失效)、保温时间不足
(5)2 Ni2+ +ClO- +4OH-= 2NiOOH↓+ Cl- + H2O

练习册系列答案
相关题目
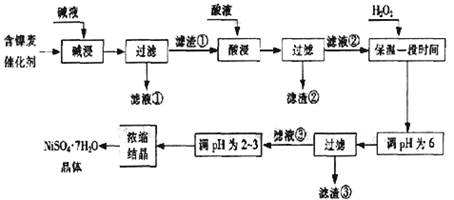
从含镍废催化剂中可回收镍,其流程如下:
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).部分阳离子以氢氧化物形式完全沉淀时的pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
(1)“碱浸”的目的是除去______.
(2)“酸浸”时所加入的酸是______(填化学式).酸浸后,滤液②中可能含有的金属离子是______.
(3)“调pH为2~3”的目的是______.
(4)产品晶体中有时会混有少量绿矾(FeSO4?7H2O),可能是由于生产过程中______.
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料--NiOOH.该反应的离子方程式是______.
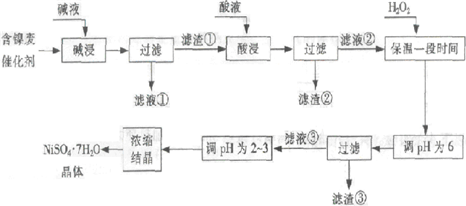
从含镍废催化剂中可回收镍,其流程如下:
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).部分阳离子以氢氧化物形式完全沉淀时的pH如下:
回答下列问题:
(1)“碱浸”的目的是除去______.
(2)“酸浸”时所加入的酸是______(填化学式).酸浸后,滤液②中可能含有的金属离子是______.
(3)“调pH为2~3”的目的是______.
(4)产品晶体中有时会混有少量绿矾,可能是由于生产过程中______.
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料--NiOOH.该反应的离子方程式是______.

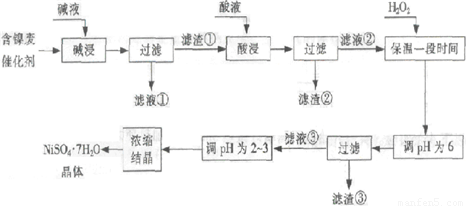
某油脂化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).部分阳离子以氢氧化物形式完全沉淀时的pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
(1)“碱浸”的目的是除去______.
(2)“酸浸”时所加入的酸是______(填化学式).酸浸后,滤液②中可能含有的金属离子是______.
(3)“调pH为2~3”的目的是______.
(4)产品晶体中有时会混有少量绿矾,可能是由于生产过程中______.
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料--NiOOH.该反应的离子方程式是______.