0 23552 23560 23566 23570 23576 23578 23582 23588 23590 23596 23602 23606 23608 23612 23618 23620 23626 23630 23632 23636 23638 23642 23644 23646 23647 23648 23650 23651 23652 23654 23656 23660 23662 23666 23668 23672 23678 23680 23686 23690 23692 23696 23702 23708 23710 23716 23720 23722 23728 23732 23738 23746 203614
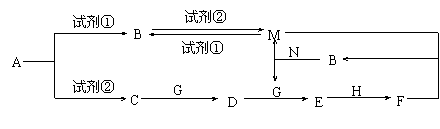 (1)A的化学式为 。
(1)A的化学式为 。