有关晶体的下列说法中正确的是( )
| A、晶体中分子间作用力越大,分子越稳定 | B、原子晶体中共价键越强,熔点越高 | C、冰融化时水分子中共价键发生断裂 | D、氯化氢溶于水时共价键不被破坏 |
有关晶体的下列说法中不正确的是( )
| A、在NaCl晶体中,距Na+最近的Cl-形成正八面体 | B、在NaCl晶体中,每个晶胞平均占有4个Na+ | C、在CsCl晶体中,每个晶胞平均占有8个Cs+ | D、铜晶体为面心立方堆积,铜原子的配位数(距离一个铜原子最近的其它铜原子的个数)为12 |
下列说法中正确的是( )
| A、CaF2晶体中F-的配位数是8,且这8个Ca2+离子呈正四面体 | B、金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | C、分子晶体的熔沸点很低,常温下都呈液态或气态 | D、原子晶体中的各相邻原子都以共价键相结合 |
下列物质的变化过程中,共价键明显被破坏的是( )
| A、I2升华 | B、溴蒸气被活性炭吸附 | C、蔗糖溶于水 | D、从NH4HCO3中闻到了刺激性气味 |
下列各组化合物中,化学键类型完全相同的是( )
| A、C2H6、H2O2、C2H5OH | B、HCl、NaCl、MgCl2 | C、H2O、CO2、Na2O2 | D、NaOH、NaClO、Na2O |
下列说法正确的是( )
| A、同主族元素的单质从上到下,熔点升高 | B、元素的最高正化合价在数值上等于它所在的族序数 | C、同周期主族元素的原子半径越小,越难失去电子 | D、元素的非金属性越强,它的气态氢化物水溶液的酸性越强 |
X、Y、Z是原子序数依次增大且属于不同周期的三种常见短周期元素,三种元素相互之间可以形成1:1型的化合物M、N、R,常温下M、N为固体,R为液体.M、N遇到水都能产生气体,而且产生的气体相互可以化合,下列说法正确的是( )
| A、R中有极性共价键和非极性共价键 | B、Z是地壳中含量最多的元素 | C、三种化合物都是共价化合物 | D、M、N投入水中所得溶液中溶质相同 |
下列有关化学用语表示正确的是( )
A、中子数为8的N原子:
| ||
B、聚丙烯的结构简式: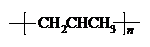 | ||
C、Cl-的结构示意图: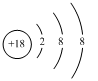 | ||
D、CSO的电子式: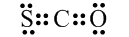 |
下列有关化学用语使用正确的是( )
A、CH4分子的比例模型: | B、H2O2的电子式: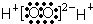 | C、硫原子的结构示意图: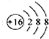 | D、醋酸的结构简式:C2H4O2 |