一定温度下,在一密闭容器中可逆反应X(g)+Y(g)?2Z(g)达到化学平衡的标志是( )
| A、单位时间内生成n mol X,同时消耗2n mol Z | B、反应体系压强不随时间而改变 | C、反应体系的平均相对分子质量不随时间而改变 | D、Y的生成速率与Z的生成速率之比为1:2 |
下列叙述正确的是( )
| A、含金属元素的离子一定都是阳离子 | B、强电解质的导电能力一定强于弱电解质 | C、原电池装置中正负极一定是两根活性不同的金属电极 | D、化学反应过程中物质变化的同时一定伴随有能量的变化 |
下列有关能量或反应热的说法正确的是( )
| A、化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 | B、牺牲阳极保护法是电能转化为化学能的过程 | C、CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol | D、放热反应一定比吸热反应更容易发生 |
信息、材料、能源被称为新科技革命的“三大支柱”.下列观点或做法错误的是( )
| A、在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源 | B、加大煤炭的开采速度,增加煤炭燃料的供应量,以缓解石油危机 | C、光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅 | D、高温结构陶瓷氮化硅(Si3N4)具有较高的硬度和耐磨性,可用于制造汽车发动机 |
下列有关说法正确的是( )
| A、△H>0的反应一定不能自发进行 | B、同温、同浓度的盐酸和氢氧化钠稀溶液中,水的电离程度相同 | C、牺牲阳极的阴极保护法和外加电流的阴极保护法都是应用电解池原理 | D、恒容密闭容器中进行的反应3A(g)?B(g)+C(g),在其他条件不变情况下,再充入一定量的A气体,A的转化率将减少 |
已知25℃、101kPa时:①2Na(s)+
O2(g)→Na2O(s)+414kJ;②2Na(s)+O2(g)→Na2O2(s)+511kJ.下列说法正确的是( )
| 1 |
| 2 |
| A、常温时,Na2O比Na2O2稳定 |
| B、①和②的产物中都只含离子键 |
| C、①和②生成等物质的量的产物,转移的电子数相同 |
| D、25℃、101kPa下,Na2O2(s)+2Na(s)→2Na2O(s)-317 kJ |
在恒容密闭容器中发生反应:A(g)+2B(g)?3C(g)+D(s),下列不能表明反应已达到化学平衡状态的标志是( )
| A、容器内气体的平均摩尔质量不随时间变化而改变 | B、容器内气体密度不随时间变化而改变 | C、容器内压强不随时间变化而改变 | D、单位时间内每生成0.5mol B的同时生成0.25mol D |
一些烷烃的燃烧热(kJ/mol)如下:
下列推断正确的是( )
| 化合物 | 燃烧热 | 化合物 | 燃烧热 |
| 甲烷 | 891.0 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 2-甲基丁烷 | 3531.3 |
| A、热稳定性:正丁烷>异丁烷 |
| B、乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)→4CO2(g)+6H2O(g)+1560.8kJ |
| C、相同质量的烷烃,碳的质量分数越大,燃烧放出的热量就越多 |
| D、正戊烷的燃烧热大约在3540kJ/mol左右 |
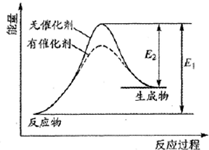 某反应过程中能量变化如图所示,下列有关叙述正确的是( )
某反应过程中能量变化如图所示,下列有关叙述正确的是( )| A、该反应为放热反应 | B、催化剂改变了化学反应的热效应 | C、催化剂不改变化学反应历程 | D、催化剂改变了化学反应速率 |