根据以下叙述,回答第21-23题
能源可划分为一级能源和二级能源.自然界中以现成形式提供的能源称为一级能源;需依靠其它能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:2H2O(液)=2H2(气)+O2(气)-517.6千焦下列叙述正确的是( )
能源可划分为一级能源和二级能源.自然界中以现成形式提供的能源称为一级能源;需依靠其它能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:2H2O(液)=2H2(气)+O2(气)-517.6千焦下列叙述正确的是( )
| A、电能是二级能源 | B、水力是二级能源 | C、天然气是一级能源 | D、焦炉气是一级能源 |
关于用水制取二级能源氢气,以下研究方向不正确的是( )
| A、构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二级能源 | B、设法将太阳光聚集,产生高温,使水分解产生氢气 | C、寻找高效催化剂,使水分解产生氢气,同时释放能量 | D、寻找特殊化学物质,用于开发廉价能源,以分解水制取氢气 |
在体积、温度都相同的条件下有下列反应:2A(气)+2B(气)?C(气)+3D(气).现分别从两条途径建立平衡:Ⅰ.A、B的起始物质的量均为2molⅡ.C、D的起始物质的量分别为2mol和6mol.以下叙述中正确的是( )
| A、Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气的百分组成相同 | ||
| B、Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气的百分组成不同 | ||
| C、达平衡时,Ⅰ途径的反应速率VA等于Ⅱ途径的反应速率VB | ||
D、达平衡时,Ⅰ途径所得混合气的密度为Ⅱ途径所得混合气密度的
|
在固定体积的密闭容器中进行如下反应:2SO2(g)+O2(g)?2SO3(g).已知反应过程某一时刻SO2,O2,SO3浓度(mol/L)分别为0.2,0.1,0.2,达到平衡时,浓度可能正确的是( )
| A、SO2为0.4mol/L | B、SO2为0.25mol/L | C、O2为0.2mol/L | D、O2为0mol/L |
反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在2L的恒容密闭容器中进行,1min后,NH3减少了0.12mol,则平均每秒钟浓度变化错误的是( )
| A、NO:0.001 mol?L-1 | B、O2:0.00125 mol?L-1 | C、NH3:0.002 mol?L-1 | D、H2O:0.0015 mol?L-1 |
下列有关物质的叙述正确的是( )
| A、沼气和天然气气都是可再生的能源 | B、盐酸和醋酸既是化合物又是酸 | C、冰和干冰即是纯净物又是化合物 | D、豆浆、牛奶和油脂都属于胶体 |
下列说法中不正确的是( )
| A、与煤油、柴油相比较,天然气是一种比较清洁的化石燃料 | B、乙醇是一种可再生能源,作为燃料的优点的是完全燃烧的产物不污染环境 | C、利用太阳能、风能和氢能等能源替代化石能源能有效改善空气质量 | D、煤的气化和液化不仅可以获得洁净燃料,而且再燃烧会放出更多的热量 |
下列说法中正确的是( )
| A、毒胶囊和老酸奶事件说明化学试剂对食品的危害,我们应该拒绝一切化学试剂的使用 | B、兴建更多的钢铁、水泥企业,提高钢铁、水泥的产量 | C、日本核泄漏造成的核辐射事故暴露出核能应用潜在的巨大危险,应立即停建核电站 | D、开发新能源,减小含碳化合物的使用,降低碳的排放 |
化学与生产、生活密切相关.下列做法合理的是( )
| A、将地沟油回收再加工为食用油,提高资源的利用率 | B、实现化石燃料的清洁利用,就无需开发新能源 | C、硅酸钠的水溶液俗称水玻璃,用它制备硅胶和木材防火剂 | D、为改善食物的色、香、味并防止变质,可在其中加入大量食品添加剂 |
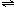 2C若维持温度和压强不变,当达到平衡时,容器的体积为V升,其中C气体的体积占10%,下列推断正确的是( )
2C若维持温度和压强不变,当达到平衡时,容器的体积为V升,其中C气体的体积占10%,下列推断正确的是( )