已知反应A+B=C+D是放热反应,对该反应的下列说法正确的是( )
| A、该反应一定属于复分解反应 | B、A的能量一定大于C | C、A和B的总能量之和一定大于C和D的总能量之和 | D、反应过程中只有化学键的形成,没有化学键的断裂 |
下列说法中正确是的( )
| A、在稀溶液中,0.55mol Ba(OH)2与l mol HNO3完全反应生成l mol H2O放出的热叫中和热 | B、将2 g NaOH固体加入到100 mL0.5 mol?L-1盐酸中,溶液导电能力变化明显 | C、中和热可表示为△H=一57.3 kJ | D、所有自发进行的反应都是放热反应 |
下列依据热化学方程式得出的结论正确的是( )
| A、已知2SO2(g)+O2?2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量 | B、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | C、已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则任何酸碱中和的反应热均为57.3 kJ | D、已知2C(s)+2O2 (g)═2 CO2(g)△H12C(s)+O2 (g)═2 CO (g)△H2则△H1<△H2 |
下列过程是非自发的是( )
| A、汽油的燃烧 | B、水由高处向低处流 | C、食物的变质 | D、室温下水结成冰 |
下列反应反应物的总能量大于生成物的总能量的是( )
| A、氢气的燃烧 | B、葡萄糖在人体内氧化分解 | C、C+H2O=CO+H2 | D、铝热反应 |
下列有关化学研究的说法,正确是( )
| A、HF的酸性弱于HCl,F的非金属性弱于Cl | B、依据丁达尔效应可将分散系分为溶液、胶体与浊液 | C、同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 | D、同时改变两个变量来研究化学反应速率的变化,能更快得出有关规律 |
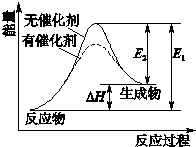 某反应的反应过程中能量变化如图所示(图中E1、E2表示反应的活化能).下列叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1、E2表示反应的活化能).下列叙述正确的是( )| A、该反应为放热反应 | B、催化剂能降低该反应的活化能 | C、催化剂能改变该反应的焓变 | D、△H=E2-E1 |
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | B、由H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1可知,若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ | C、300℃、30MPa下,将0.5molN2(g)和1.5mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)=2NH3(g)△H=-38.6kJ?mol-1 | D、由C(石墨)═C(金刚石)△H=+1.90 kJ?mol-1可知,金刚石比石墨稳定 |
下列表示吸热反应的图象是( )
A、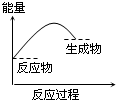 | B、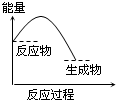 | C、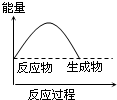 | D、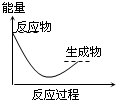 |
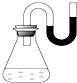 把下列物质分别加入装有水的锥形瓶里立即塞紧装有U形管的塞子,已知U形管内预先装有少量水(为使水容易观察,预先染成红色).如图所示,结果U型管右边液面升高,则加入的物质可能是( )
把下列物质分别加入装有水的锥形瓶里立即塞紧装有U形管的塞子,已知U形管内预先装有少量水(为使水容易观察,预先染成红色).如图所示,结果U型管右边液面升高,则加入的物质可能是( ) ①NaOH固体 ②浓H2SO4 ③NH4NO3晶体 ④Na2O2 ⑤生石灰.
| A、①②④⑤ | B、①②③ | C、②③⑤ | D、③④⑤ |