下列实验能达到预期目的是( )
| A、向某无色液中加入BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有SO42- | B、向CuSO4溶液中加入稍过量的NaOH溶液,得到Cu(OH)2悬浊液,再加入适量蔗糖加热有红色沉淀生成,说明蔗糖分子结构中有醛基 | C、取醋酸钠溶液,用PH试纸检验,试纸变蓝,说明醋酸是弱酸 | D、将淀粉溶液和食盐溶液混合装入半透膜,浸入纯水中,过一段时间,取半透膜内的液体滴入碘水呈蓝色,说明利用渗析可提纯胶体 |
臭氧分子的结构与SO2(极性分子)相似,可读做二氧化氧,在臭氧层中含量达0.2ppm(ppm表示百万分之一).臭氧是氧气吸收了太阳的波长小于242nm的紫外线形成的,不过当波长在220nm~320nm的紫外线照射臭氧时,又会使其分解.下列说法中正确的是( )
| A、向大气中排放氮的氧化物和氟氯代烃均能加快臭氧的分解 | B、臭氧转化为氧气和氧气转化为臭氧均须吸收能量 | C、臭氧和氧气的相互转化能保持大气中臭氧的含量基本稳定 | D、打雷时也能产生臭氧,臭氧分子是直线型分子 |
下列关于浓硝酸和浓硫酸的叙述,正确的是( )
①常温下都能用铝制容器贮存
②常温下都能与铜较快反应
③露置在空气中,容器内酸液的质量都减少
④露置在空气中,容器内酸液的浓度均降低.
①常温下都能用铝制容器贮存
②常温下都能与铜较快反应
③露置在空气中,容器内酸液的质量都减少
④露置在空气中,容器内酸液的浓度均降低.
| A、①③ | B、①④ | C、②③ | D、②④ |
德国化学家格哈德?埃特尔获得2007年度诺贝尔化学奖,因他在“固体表面化学过程”研究中作出的贡献.表面化学反应在工农业操作中有着重要作用:金属表面暴露在潮湿的空气中时生锈;电子工业中,制作半导体元件.下列有关叙述正确的是( )
| A、二氧化硅的导电性介于导体和绝缘体之间,是半导体材料 | B、二氧化硅制作的光导纤维非常细,导光能力很强 | C、纯净的硅酸钠晶体俗称“水玻璃” | D、玻璃在加热熔化时有固定的熔点 |
下列有关实验操作或现象中,正确的是( )
| A、将新配制的0.1mol?L-1的NaOH溶液转移到干燥、洁净、带橡胶塞的无色细口瓶中 | B、向溶液中通入足量的氯气,以除去Fe2(SO4)3溶液中FeSO4 | C、在中和滴定实验过程中,目光应密切注视滴定管中的液面变化 | D、在电压的作用下,液晶分子能沿电场方向排列,移去电场后,液晶分子仍能沿电场方向排列 |
下列说法中,正确的是( )
| A、电解精炼铜时,粗铜中的金、银、锌等形成阳极泥而与铜分离 | B、易潮解的试剂都要用带磨口玻璃塞的广口瓶保存 | C、氨可将NO2转化成无毒的物质,是因为氨具有还原性 | D、用己知浓度的盐酸滴定锥形瓶中未知浓度的氢氧化钠溶液时,若锥形瓶中原残留有少量蒸馏水,滴定结果将偏低 |
下列叙述中不正确的是( )
| A、硅和锗均可作半导体材料 | B、CO2和SiO2都是酸性氧化物,都能和水反应 | C、C、Si和Ge的最外层电子数都是4 | D、SiO2和CO2中,Si和O、C和O之间都是共价键 |
下列对实验现象的预测不正确的是( )
| A、向氢氧化铁胶体中滴加盐酸至过量,开始有沉淀出现,后来沉淀又溶解 | B、向Na2SiO3溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 | C、向Ca(ClO)2溶液中通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | D、向Ca(OH)2溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入过量NaOH溶液,又变浑浊 |
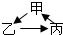 ”(“→”表示一步反应)的是( )
”(“→”表示一步反应)的是( )